
【题目】下列有关说法正确的是
A. 已知HI(g) ![]() 1/2H2(g)+1/2I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量
1/2H2(g)+1/2I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量
B. 已知2H2(g)+O2(g)===2H2O(g) ΔH=-571.6 kJ·mol-1,则氢气的燃烧热为ΔH=-285.8 kJ·mol-1
C. 已知2C(s)+2O2(g)=2CO2(g) ΔH1, 2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2
D. 含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)===CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ·mol-1
【答案】C
【解析】
A. HI(g) ![]() 1/2H2(g)+1/2I2(s) ΔH=-26.5 kJ·mol-1,由于反应可逆,可知1 mol HI气体充分分解后可以放出小于26.5 kJ的热量,故A错误;
1/2H2(g)+1/2I2(s) ΔH=-26.5 kJ·mol-1,由于反应可逆,可知1 mol HI气体充分分解后可以放出小于26.5 kJ的热量,故A错误;
B.根据燃烧热定义可知,水的状态不对,必须为液态才可以,故B错误;
C.已知2C(s)+2O2(g)=2CO2(g) ΔH1, 2C(s)+O2(g)=2CO(g) ΔH2,盖斯定律可得:2CO(g)+O2(g)= 2CO2(g) ΔH1-ΔH2,因为燃烧放热,所以ΔH1-ΔH2<0, 则ΔH1<ΔH2,故C正确;
D.因为醋酸为弱电解质,电离需要吸热,所以NaOH(aq)+CH3COOH(aq)==CH3COONa(aq)+H2O(l) ΔH>-57.4 kJ·mol-1,故D错误;
正确答案:C。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,下列操作会引起实验结果偏大的是
A. 滴定前,滴定管尖嘴有气泡,滴定后无气泡
B. 在锥形瓶装液前,留有少量蒸馏水
C. 锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D. 用酸式滴定管量取液体时,读数,之前俯视,之后平视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜是化工和印染等行业的重要原料,广泛用作有机合成的催化剂。
Ⅰ.甲采用CuCl2·2H2O热分解法制备CuCl,装置如图。

(1)仪器X的名称是_______________,C中烧杯的试剂可以是__________。
(2)“气体入口”通入的气体是_______。
(3)反应结束后,取所得产品分析,发现其中含有氧化铜,其可能原因是______________。
Ⅱ.乙另取纯净CuCl2固体用如下方法制备CuCl。

(4)操作②中反应的离子方程式为___________________。
(5)操作①中若用100 mL 10 mol/L盐酸代替0.2 mol/L盐酸,再通入SO2后,无白色沉淀产生。对此现象有如下两种猜想:
猜想一:c(H+)过大导致白色沉淀溶解。为验证此猜想,取75gCuCl2固体、100 mL0.2 mol/L盐酸及________mL10.0mol/LH2SO4配制成200 mL溶液,再进行操作②,观察是否有白色沉淀产生。
猜想二:_______________。请设计实验说明该猜想是否成立:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(H2NCOONH4)是一种易水解、受热易分解的白色固体,某研究小组用下图所示的实验装置制备氨基甲酸铵,反应原理为:2NH3(g)+CO2(g)=H2NCOONH4(s) △H<0。

(1)仪器B的名称是________________。
(2)打开阀门K,装置E中由固体药品所产生的气体就立即进入装置D,则该固体药品的名称为________________。
(3)装置D为制备氨基甲酸铵的反应器(CCl4充当惰性介质),在合适催化剂下搅拌一段时间。
①反应在冰水浴中进行的原因为_______________________________________。
②当CCl4液体中产生较多晶体悬浮物时,即停止反应,__________(填操作名称)分离得到粗产品。
(4)仪器G的作用有:_______________________________________。
(5)该实验装置中有一处不足,改进方法是______________________________________。
(6)已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式_________________。
(7)为测定某样品中氨基甲酸铵的质量分数,某研究小组用该样品进行实验,已知杂质不参与反应,请补充完整测定某样品中氨基甲酸铵质量分数的实验方案(限选试剂:蒸馏水、澄清石灰水、Ba(OH)2溶液):用天平称取一定质量的样品,加水溶解,____________________,测量的数据取平均值进行计算。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 |
HClO | 3×10-8 |
H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
H2C2O4 | K1=5.4×10-2 K2=5.4×10-5 |
H2S | K1=1.3×10-7 K2=7.1×10-15 |
请回答下列问题:
(1)同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是____。
(2)常温下0.1 mol/L的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填字母)。
A.c(H+) B.![]() C.
C.![]() D.c(OH-)
D.c(OH-)
(3)0.1 mol/L的H2C2O4溶液与0.1mol/L的KOH的溶液等体积混合后所得溶液中各离子浓度由大到小的顺序为__________________。
(4)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是CH3COOK________NaClO (填“>”、“<”或“=”)。
(5)向0.1mol/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=______________。
(6)向NaClO溶液中通入少量的CO2,所发生的离子方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4C1、FeC13、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是_____________(写化学式)。
(2)写出并配平该反应的化学方程式。__________________________________
(3)发生氧化反应的物质是____________,反应中4mol的氧化剂能_______(填“失去”或“得到”)_________________mol电子.
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活生产密切相关。下列说法中不正确的是
A. 施肥时,铵态氮肥不能与草木灰(含K2CO3)混合使用
B. 夏天冰箱保鲜食品的原理是降低温度,减小化学反应速率
C. 施用适量石膏(CaSO4·2H2O)可降低盐碱地(含较多NaCl、Na2CO3)的碱性
D. 将海水直接电解可获得 Mg及Cl2等单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温(500K)、体积为2.0L的密闭容器中通入1.0molN2和1molH2发生合成氨反应,20min后达到平衡,测得反应放出的热量为18.4kJ,混合气体的总物质的量为1.6mol。
(1)从开始反应至达到平衡时,用NH3表示该反应的化学反应速率v(NH3)=______。
(2)该反应的热化学方程式为______。
(3)若拆开1molH—H键和1molN![]() N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是______kJ。
N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是______kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)![]() pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
①m+n>p ②x点表示的正反应速率大于逆反应速率
③x点比y点时的反应速率慢 ④n>p
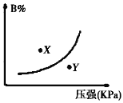
A. ①② B. ②④ C. ②③ D. ①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com