
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| c��NO���� mol•L-1�� | 1.00��10-3 | 4.50��10-4 | 2.50��10-4 | 1.50��10-4 | 1.00��10-4 | 1.00��10-4 |
| c��CO���� mol•L-1�� | 3.60��10-3 | 3.05��10-3 | 2.85��10-3 | 2.75��10-3 | c | 2.70��10-3 |
���� ��1���ɷ���ʽ��֪2molNO��2molCO��Ӧ����2molCO2��1molN2���ʸ÷�ӦΪ�ؼ��ķ�Ӧ�����ݡ�G=��H-T��S��0����Ӧ�����Է����У��ݴ��жϣ�
��2�����淴Ӧ����ƽ��ʱ��ͬһ���ʱ�ʾ�����淴Ӧ������ȣ�����ֵ�Ũ�ȡ��������䣬�ɴ�����������һЩ�����䣬�ж�ƽ��״̬��������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����仯��˵������ƽ�⣻
��3����Ҫ�ӿ췴Ӧ������Ҫ���NOת���ʣ�ƽ�������ƶ�������ӦΪ���������С����������ѹǿ����������CO��Ũ�ȣ������¶ȣ���Ӧ���ʼӿ죬��Ϸ�Ӧ��ЧӦƽ��ƽ���ƶ������ж�NOת���ʱ仯��
��4�����ɱ������ݿ�֪��4s��5sʱNO��Ũ����ȣ�˵��4sʱ��Ӧ����ƽ�⣻
�ڸ���v=$\frac{��c}{��t}$����ǰ2s��v��NO��������������֮�ȵ����仯ѧ������֮�ȼ���v��N2����
����������ʽ����ƽ��ʱ����ֵ�ƽ��Ũ�ȣ�����ƽ�ⳣ������ʽK=$\frac{{c}^{2}��C{O}_{2}����c��{N}_{2}��}{{c}^{2}��NO����{c}^{2}��CO��}$���㣮
��� �⣺��1���ɷ���ʽ��֪2molNO��2molCO��Ӧ����2molCO2��1molN2���ʸ÷�ӦΪ�ؼ��ķ�Ӧ�������¸÷�Ӧ�����Է����У����ݡ�G=��H-T��S��0����Ӧ�����Է����У��ʡ�H��0��
�ʴ�Ϊ������
��2��A���¶ȡ�������䣬�淴Ӧ���л�����������ʵ�����С������ѹǿ��С����������ѹǿ���ֲ��䣬˵����Ӧ����ƽ�⣬��A��ȷ��
B��������N2��Ũ�Ȳ��ٸı䣬˵����Ӧ����ƽ�⣬��B��ȷ��
C������CO�����ʵ���������CO2�����ʵ���֮��Ϊ1��1������ʾ����Ӧ���ʣ���Ӧ��ֵ���˱������У�����˵������ƽ�⣬��C����
D��ƽ��ʱ����ֵ����ʵ���֮�Ȳ�һ�����ڻ�ѧ������֮�ȣ������ʵ���ʼ���ʵ�����ת�����йأ���D����
��ѡ��AB��
��3��A��ѡ�ø���Ч�Ĵ������ӿ췴Ӧ���ʣ����̵���ƽ���ʱ�䣬��Ӱ��ƽ���ƶ���NO��ת���ʲ��䣬��A����
B�����߷�Ӧ��ϵ���¶ȣ���Ӧ���ʼӿ죬����ӦΪ���ȷ�Ӧ����Ӧ���淴Ӧ�����ƶ���NO��ת���ʽ��ͣ���B����
C�����ͷ�Ӧ��ϵ���¶ȣ�ƽ��������Ӧ�����ƶ���NO��ת����������Ӧ���ʽ��ͣ���C����
D������ӦΪ���������С�ķ�Ӧ����С�����������ѹǿ����Ӧ���ʼӿ죬ƽ��������Ӧ�����ƶ���NO��ת��������D��ȷ��
��ѡ��D��
��4�����ɱ������ݿ�֪��4s��5sʱNO��Ũ����ȣ�˵��4sʱ��Ӧ����ƽ�⣬��c=2.70��10-3mol/L��
�ʴ�Ϊ��2.70��10-3��
���ɱ������ݿ�֪��ǰ2s��NOŨ�ȱ仯��Ϊ1.0��10-3mol/L-2.50��10-4mol/L=7.5��10-4mol/L����2s��v��NO��=$\frac{7.5��1{0}^{-4}mol/L}{2s}$=3.75��10-4mol/��L��s��������֮�ȵ����仯ѧ������֮�ȣ�v��N2��=$\frac{1}{2}$v��NO��=$\frac{1}{2}$��3.75��10-4mol/��L��s��=1.875��10-4mol/��L��s����
�ʴ�Ϊ��1.875��10-4mol/��L��s����
��ƽ��ʱ��NO��Ũ��Ϊ1.0��10-4mol/L����
2 NO��g��+2 CO��g��?2 CO2��g��+N2��g��
��ʼ��mol/L����1.0��10-3 3.6��10-3 0 0
ת����mol/L����9��10-49��10-4 9��10-4 4.5��10-4
ƽ�⣨mol/L����1.0��10-427��10-49��10-44.5��10-4
ƽ�ⳣ������ʽK=$\frac{{c}^{2}��C{O}_{2}����c��{N}_{2}��}{{c}^{2}��NO����{c}^{2}��CO��}$=$\frac{��9��1{0}^{-4}��^{2}��4.5��1{0}^{-4}}{��1.0��1{0}^{-4}��^{2}����27��1{0}^{-4}��^{2}}$=5��103��
�ʴ�Ϊ��5��103��
���� ���⿼��ƽ��״̬�жϡ���ѧƽ���ƶ�����ѧƽ����㡢��ѧ��Ӧ���ʼ��㡢ƽ�ⳣ������ȣ����ؿ���ѧ������������������Ҫѧ���߱���ʵ�Ļ������Ѷ��еȣ�


 ȫ��������ϵ�д�
ȫ��������ϵ�д� һ��һ����ʱ���ϵ�д�
һ��һ����ʱ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | CH4 | CO2 | CO | H2 |
| ƽ��Ũ�ȣ�mol•L-1�� | 0.5 | 1.0 | 1.0 | 1.0 |
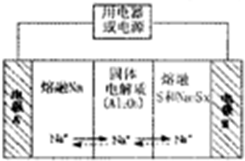
| ���� | Na | S | Al2O3 |
| �۵�/�� | 97.8 | 115 | 2050 |
| �е�/�� | 892 | 444.6 | 2980 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C3H6 | B�� | C5H12 | C�� | C6H4Cl2 | D�� | C4H8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ˮ��������Cl2������ԭ����ȫ��ͬ | |
| B�� | �÷�Ӧ��������������ClO-������ǿ��FeO42- | |
| C�� | ������Ӧ��Fe��0H��3��ClO-�����ʵ���֮��ӦΪ3��2 | |
| D�� | ��ΪFeO32-��ֱ��ˮ�����������������壬�ʿ�������ˮ�ľ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
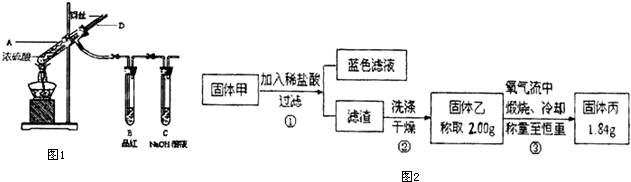
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȣ�SrSO4����������ˮ�İ�ɫ���� | |
| B�� | ����At��Ϊ��ɫ���壬HAt���ȶ���AgAt�й��Ժ�ǿ����������ˮҲ�������� | |
| C�� | �����⣨H2Se������ɫ���ж������壬��H2S�ȶ� | |
| D�� | �루Be�����������ˮ������ܾ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ֻ��1�����ӵ�Ԫ��һ���ǽ���Ԫ�� | |
| B�� | �����ֻ��2�����ӵ�Ԫ��һ���ǽ���Ԫ�� | |
| C�� | ԭ�Ӻ�������������ȵ�Ԫ��һ���ǽ���Ԫ�� | |
| D�� | �˵����Ϊ17��Ԫ�ص�ԭ�ӵ�������һ����35 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com