
硝基苯是重要的精细化工原料,是医药和染料的中间体,还可做有机溶剂。制备硝基苯的过程如下:①配制混酸:组装如下图反应装置。
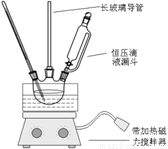
取100 mL烧杯,用20 mL浓硫酸与浓硝酸18 mL配制混和酸,加入漏斗中。把18 mL苯加入三颈烧瓶中。
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。
③在50-60℃下发生反应,直至反应结束。
④除去混和酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品。
已知(1)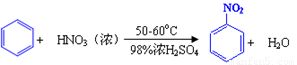
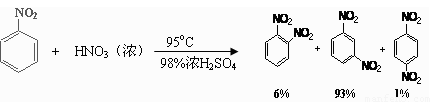
(2)可能用到的有关数据列表如下
|
物质 |
熔点/℃ |
沸点/℃ |
密度(20 ℃) / g·cm-3 |
溶解性 |
|
苯 |
5.5 |
80 |
0.88 |
微溶于水 |
|
硝基苯 |
5.7 |
210.9 |
1.205 |
难溶于水 |
|
1,3-二硝基苯 |
89 |
301 |
1.57 |
微溶于水 |
|
浓硝酸 |
|
83 |
1.4 |
易溶于水 |
|
浓硫酸 |
|
338 |
1.84 |
易溶于水 |
请回答下列问题:
(1)配置混酸应先在烧杯中先加入 。
(2)恒压滴液漏斗的优点是 。
(3)实验装置中长玻璃管可用 代替(填仪器名称)。
(4)反应结束后产品在液体的 层(填“上”或者“下”),分离混酸和产品的操作方法为 。
(5)用10%Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净? 。
(6)为了得到更纯净的硝基苯,还须先向液体中加入 除去水,然后蒸馏,
(1)浓硝酸
(2)可以保持漏斗内压强与发生器内压强相等,使漏斗内液体能顺利流下
(3)冷凝管(球形冷凝管或直行冷凝管均可)
(4)上 分液
(5)取最后一次洗涤液,向溶液中加入氯化钙,无沉淀生成,说明已洗净。
(6) 氯化钙
【解析】
试题分析:(1)由于浓硫酸的密度比浓硝酸的大,当浓硫酸遇水时放出大量的热,所以配置混酸应将浓硫酸加入到浓硝酸中,也就是先在烧杯中先加入浓硝酸。(2)由于在反应的过程中不断加热,会产生大量的气体,这对于液体的加入很不利。若采用恒压滴液漏斗滴加,可以保持漏斗内压强与发生器内压强相等,使漏斗内液体能顺利流下。(3)在实验的过程中苯、硝酸会因为加热而气化,导致物质的浪费与环境污染,所以在装置中长玻璃管可以起到冷凝、降温使物质回流的作用。因此可用冷凝管等冷凝装置代替。(4)反应结束后产生的硝基苯、1,3-二硝基苯都不溶解于水的液体,密度比酸的混合溶液小。所以反应结束后产品在液体的上层,分离互不相溶的两层液体的方法是分液。(5)对于得到的粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤。如果洗涤干净,则洗涤液中不含有CO32-。所以检验液体已洗净的方法是取最后一次洗涤液,向溶液中加入氯化钙,若无沉淀生成,说明已洗净。(6)为了得到更纯净的硝基苯,使之不含有水,可以先向液体中加入有吸水干燥作用的无水CaCl2,除去水,然后蒸馏。就得到了产品。
考点:考查重要的精细化工原料硝基苯的制取过程中涉及的物质的混合、混合物的分离、物质的洗涤、检验等实验操作等知识。


科目:高中化学 来源: 题型:
| A、常温常压下,密度比水的小 | B、分子中含有3个碳碳双键 | C、不能在空气中燃烧 | D、能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
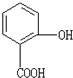
| A、分子式是C7H7O3 | B、可以与NaOH反应,但不能与Na2CO3反应 | C、能发生取代反应和加成反应 | D、它的同分异构体可以是酯类 |
查看答案和解析>>
科目:高中化学 来源: 题型:
水杨酸是重要的精细化工原料,它的结构简式为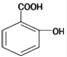 .水杨酸的芳香族同分异构体 ( )
.水杨酸的芳香族同分异构体 ( )
A.可能含有两个醛基 B.可能含有三个羟基
C.都能溶于氢氧化钠溶液 D.分子式都是C7H7O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com