
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是________________
(2)实验室中现有Na2SO4、CuCl2、MgSO4、K2SO4等4种溶液,可与上述实验中CuSO4
溶液起相似作用的是________;
(3)要加快上述实验中气体产生的速率,还可采取的措施有________________(答两种)
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,
收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol/L H2SO 4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液 /mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O /mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1= ,V6= ,V9= ;
② 该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
常温下,若HA溶液和NaOH溶液混合后pH=7,下列说法不合理的是( )
A. 反应后HA溶液可能有剩余
反应后HA溶液可能有剩余
B.生成物NaA的水溶液的pH可能小于7
C.HA溶液和NaOH溶液的体积一定相等
D.HA溶液的c(H+)和NaOH溶液的c(OH-)可能不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A.相对分子质量相同的有机物是同分异构体
B.烷烃分子中,相邻的三个碳原子有可能在同一条直线上
C.每个碳原子的化合价都已“饱和”,碳原子之间只以单键相结合的链烃一定是烷烃
D.分子组成上相差一个或若干个CH2原子团的物质,互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,美国正在研究的锌电池可能取代目前广泛使用的铅蓄电池。锌电池具有容量大、污染少等优点。电池反应为2Zn+O2=2ZnO,原料为锌粒、电解液和空气。下列叙述正确的是
A.锌为正极,空气进入负极反应
B.负极反应为Zn+2OH--2e-=ZnO+H2O
C.正极发生氧化反应
D.电解液肯定是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室常用NaNO2和NH4Cl反应制取N2。下列有关说法正确的是
A.NaNO2是还原剂
B.NH4Cl中N元素被还原
C.生成1 mol N2时转移6 mol电子
D.氧化剂和还原剂的物质的量之比是1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
N2O俗称“笑气”,曾用作可吸入性麻醉剂。以下反应能产生N2O:3CO+2NO2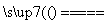 3CO2+N2O。下列关于N2O的说法正确的是
3CO2+N2O。下列关于N2O的说法正确的是
A.上述反应中每生成1 mol N2O,消耗1.5 mol CO
B.等物质的量的N2O和CO2含有相等的电子数
C.N2O只具有氧化性,无还原性
D.N2O会迅速与人体血红蛋白结合,使人中毒
查看答案和解析>>
科目:高中化学 来源: 题型:
化学是以实验为基础的自然科学,化学实验设计和操作中必须十分重视师生安全问题和环境保护问题。下列实验问题处理方法不正确的是( )
A.制氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
B.在气体发生装置上直接点燃乙烯气体时,必须先检验乙烯气体的纯度
C.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
D.给试管中的液体加热时不时地移动试管或加入碎瓷片,以免暴沸伤人
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。
通过测定反应过程中所放出的热量可计算中和热。回答下列问题
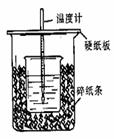 (1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(3)已知在稀溶液中,强酸和强碱发生中和反应生成1mol H2O时, 放 出57.3kJ的热量,则上述反应的热化学方程式为_________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com