
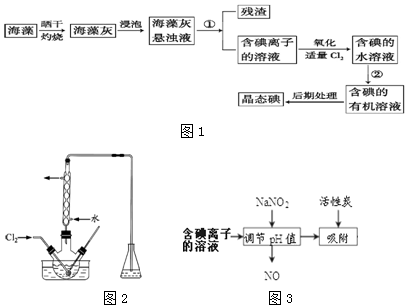
���� ����ɹ�����տ�����ˮ�Ͷ�����̼���������к��е⻯�ص����ʣ�����ˮ�����ݹ��˵õ����е����ӵ���Һ��������ˮ��ͨ�������������û����⣬�õ����ˮ��Һ�������Ȼ�̼��ȡ�õ�������л���Һ��������ɵõ��⣬
��1����������Һ���ù��ˣ���һ���ܼ������ʴ�������һ���ܼ�����ɵ���Һ����ȡ��������ȡ��
��2���������������������ܽ�������¶ȵ����߶���С�����������������ܺ�����������Һ��Ӧ���������ʣ�
��3����ȡ�Ļ���ԭ�������ܼ��������ܣ���������һ���ܼ��е��ܽ�ȱ�����һ�ִ�Ķ࣬�ݴ���ѡ����ʵ��Լ���
��4����NaNO2�������ԣ�����I-����ΪI2����������ԭΪNO��
�����������ɵ�NOβ���ж�����ҵ�Ͻ�����O2��һ������ͨ��NaOH�Ʊ�NaNO2�����ݵ����غ㼰Ԫ���غ�ɵ÷�Ӧ�Ļ�ѧ����ʽ��
��5�������Ӿ���������������������Ϊ�ⵥ�ʣ���Ϸ�Ӧ������ϵ���㣮
��� �⣺��1����ȡ��Ĺ����Тٷ��������Թ����������Һ�������ʵ����������ǹ��ˣ����ǰѵⵥ�ʴӵ�ˮ�з�����ȡ������л�����Һ��ȥ���������õ����������л������ˮ���ܽ�Ƚ�С��ˮ���л��ﻥ�����ܵ��ص㣬������ȡ�ķ��������ᴿ��
�ʴ�Ϊ�����ˣ���ȡ��
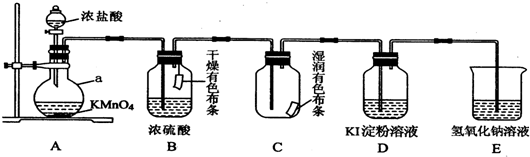
��2������ʱ����������ƿ�н���I-��ˮ��Һ���������pHԼΪ2������ͨ��Cl2����40�����ҷ�Ӧ��ʵ������ڽϵ��¶��½��е�ԭ���Ƿ�ֹ������������ʹ��������ܽⷴӦ��Cl2�Ǵ�����Ⱦ����ŷ�֮ǰҪ����β����������NaOH��Һ�����գ���ƿ�����Ӧ�����ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ����ֹ������������ʹ��������ܽⷴӦ��Cl2+2OH-=Cl-+ClO-+H2O��
��3���ڵڢڲ����������У��ɼ�����й��Լ�����ˮ�������ܵ��л��
A���ƾ���ˮ���ܣ�����ʹ�ã���A����
B�����Ȼ�̼��ˮ�������ܣ���B��ȷ��
C��������������ˮ����C����
D������ˮ�������ܣ���D��ȷ��
�ʴ�Ϊ��BD��
��4����NaNO2�������ԣ�����I-����ΪI2��ͬʱ������ǿ�������Σ�ˮ��Һ�Լ��ԣ�Ҳ���Ե�����Һ������ԣ�����NaNO2������pH��4����Ӧ�����ӷ���ʽ�ǣ�2NO2-+4H++2I-=2NO��+I2+2H2O��
�ʴ�Ϊ��2NO2-+4H++2I-=2NO��+I2+2H2O��
�����������ɵ�NOβ���ж�����ҵ�Ͻ�����O2��һ������ͨ��NaOH�Ʊ�NaNO2�����ݵ����غ㼰Ԫ���غ�ɵ÷�Ӧ�Ļ�ѧ����ʽΪ4NaOH+O2+4NO=4NaNO2+2H2O��
��5�������Ӿ���������������������Ϊ�ⵥ�ʷ�Ӧ�ķ���ʽ�ǣ�2Fe3++2I-=2Fe2++I2��
n��Fe3+��=0.1mol/L��0.0204L=2.04��10-3mol��
����n��I-��=2.04��10-3mol��
�����ӵ���Һ��I-��Ũ��Ϊc��I-��=$\frac{n��{I}^{-}��}{V}$=2.04��10-3mol��$\frac{2.04��1{0}^{-3}mol}{0.025L}$=0.082mol/L��
�ʴ�Ϊ��0.082mol/L��
���� ������Ҫ�����˹�ҵ�Ʊ�����������ˮ�⡢������ԭ��Ӧ�����ӵļ��顢���ʵķ�����ᴿ��֪ʶ�㣬��Ŀ�Ѷ��еȣ�Ԫ�ص��ƶ��ǽ���Ĺؼ���


 �ľ�ͼ���ʱ�ȷ�ϵ�д�
�ľ�ͼ���ʱ�ȷ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 17g NH3���е�����Ϊ10NA | |
| B�� | ����£�4.48LH2O�������ķ�������0.2NA | |
| C�� | 0.1mol/L��K2SO4��Һ�У�K+����ĿΪ0.2NA | |
| D�� | 30 g���飨C2H6��������ԭ����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���壮
�о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2H2��g��+O2��g���T2H2O��1����H=-571.6kJ/mol | B�� | 2H2��g��+O2��g���T2H2O��1����H=+571.6 kJ/mol | ||
| C�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-285.8 kJ/mol | D�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��1����H=-285.8kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ҡ�� | B�� |  ����Һ���� | C�� |  �μ�Һ�� | D�� |  ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | V��=V����V�� | B�� | V����V����V�� | C�� | V����V����V�� | D�� | V��=V��=V�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
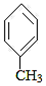 +CO$��_{��}^{AlCl_{3}��HCl}$
+CO$��_{��}^{AlCl_{3}��HCl}$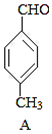 $��_{OH-����}^{CH_{3}CHO}$B$��_{��H+}^{��C}$
$��_{OH-����}^{CH_{3}CHO}$B$��_{��H+}^{��C}$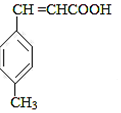 $��_{Ũ���ᣬ��}^{CH_{3}OH}$E
$��_{Ũ���ᣬ��}^{CH_{3}OH}$E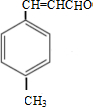 ������E�ķ�Ӧ����Ϊ������Ӧ��ȡ����Ӧ
������E�ķ�Ӧ����Ϊ������Ӧ��ȡ����Ӧ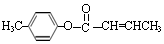 ��E��һ��ͬ���칹�壬������������NaOH��Һ���ȵĻ�ѧ����ʽΪ
��E��һ��ͬ���칹�壬������������NaOH��Һ���ȵĻ�ѧ����ʽΪ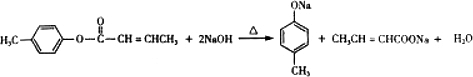 ��
��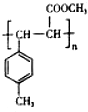 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com