
【题目】氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置______。![]() 的中子数为________。
的中子数为________。
已知:P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;由此推知,其中最稳定的磷单质是________。
(2)氮和磷氢化物性质的比较:热稳定性:NH3________PH3(填“>”或“<”)。沸点:N2H4________P2H4(填“>”或“<”),判断依据是____________。
【答案】第四周期ⅤA族 173 黑磷 > > N2H4分子间存在氢键
【解析】
(1)As位于第四周期第VA族,中子数=质量数-质子数;能量越低越稳定;
(2)元素的非金属性越强,其氢化物越稳定;分子晶体熔沸点与分子间作用力和氢键有关,能形成分子间氢键的氢化物熔沸点较高。
(1)As位于第四周期第VA族,中子数=质量数-质子数=288-115=173;
能量越低越稳定,
P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1①
P(s,白磷)=P(s,红磷)ΔH=-17.6 kJ·mol-1②
将方程式①-②得![]() ,
,
则能量:红磷>黑磷,则黑磷稳定,
故答案为:第四周期第VA族;173;黑磷;
(2)元素的非金属性越强,其氢化物越稳定;
非金属性N>P,所以热稳定性:NH3>PH3;
N2H4能形成分子间氢键、P2H4分子间不能形成氢键,所以沸点:N2H4>P2H4,
故答案为:>;>;N2H4分子间存在氢键。


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
【题目】下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A. Fe + CuSO4 = FeSO4+ Cu
B. AgNO3+ NaCl= AgCl↓ + NaNO3
C. MnO2 + 4 HCl(浓) ![]() MnCl2+ Cl2↑ + 2 H2O
MnCl2+ Cl2↑ + 2 H2O
D. 2KMnO4 ![]() K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国不少古诗词清晰描述了当时人们的生活和社会的发展,如刘禹锡的《浪淘沙》“日照澄洲江雾开,淘金女伴满江隈,美人首饰侯王印,尽是沙中浪底来。”下列有关本诗中蕴含的化学知识认知正确的是
A.雾的分散质粒子直径范围是1~100nmB.淘金原理与化学上的萃取一致
C.沙子的主要成分是![]() D.“沙中浪底来”指的是金的氧化物
D.“沙中浪底来”指的是金的氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是
A.下图是在不同温度下三个恒容容器中反应2H2(g)+CO(g)CH3OH(g) △H<0的平衡曲线,曲线X对应的温度相对较高
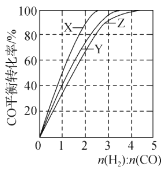
B.下图是一定温度下三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线,a点可表示MgCO3的过饱和溶液,且c(Mg2+)>c(CO32-)
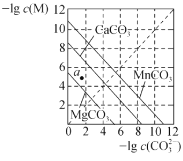
C.下图为MOH和ROH两种一元碱水溶液在常温下分别加水稀释时pH值的变化曲线,可知ROH是强碱
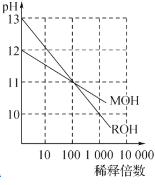
D.下图为两个1L容器中各投入1molCH4和1molCO2所发生反应CH4(g)+CO2(g)2CO(g)+2H2(g)的平衡曲线,N点化学平衡常数K=1
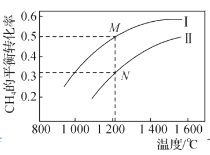
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
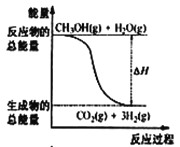
①CH3OH(g)+H2O(g) = CO2(g)+3H2(g) △H=+49. 0 kJ·mol-1
②CH3OH(g)+![]() O2(g) = CO2(g)+2H2(g) △H=-192. 9 kJ·mol-1
O2(g) = CO2(g)+2H2(g) △H=-192. 9 kJ·mol-1
下列说法正确的是
A.CH3OH的燃烧热为192. 9 kJ·mol-1
B.根据②推知反应:CH3OH(l) +![]() O2(g) =CO2(g) +2H2(g) △H >-192. 9kJ·mol-1
O2(g) =CO2(g) +2H2(g) △H >-192. 9kJ·mol-1
C.CH3OH转变成H2的过程一定要吸收能量
D.反应①中的能量变化如图所示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类应用较早, 当前应用量最大的金属元素,下列有关铁及其化合物的有关说法中不正确的是( )
A.磁铁矿的主要成分是Fe3O4
B.铁与水蒸气在高温下的反应产物为Fe3O4和H2
C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加入足量铁粉后过滤
D.Fe3与KSCN 溶液产生红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属的冶炼方法有很多,有加热法,热还原法、 电解法、湿法冶金等:我国古代利用铁和硫酸铜溶液反应炼铜,属于___(填冶炼的方法);铝热反应是铝与一些金属氧化物在高温下反应,属于___(填冶炼的方法);写出铝与四氧化三铁的反应方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】层状复合金属氢氧化物(简称“层状氢氧化物”),主体层板由二元(或多元)金属氢氧化物层构成,层间阴离子可以被其他阴离子取代,因此可以作为离子交换剂,在材料、化工、医药和环境保护等方面有着广泛的用途。镁铝碳酸根型水滑石是人们最早发现的层状氢氧化物。回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最小的是___________(填标号)。
A. B.
B. C.
C.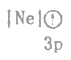 D.
D.
(2)一种水滑石的化学式为Mg4Al2(OH)12CO3H2O.其层板结构如图1。CO32-中碳的杂化类型是____。在图中最小的一个二维菱形晶胞(以图中Al为顶点)中含有___________个Al3+。每个镁氧八面体周围有_______________个相邻铝氧八面体和_______________个相邻镁氧八面体。
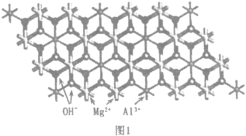
(3)水滑石中氢氧化物层的OH-和层间阴离子间的主要作用力为_______________,水滑石作为离子交换剂,去除水体中阴离子去除效果依次为:PO43->CrO42->NO3-,其原因是___________
(4)当加热到一定温度时,水滑石类化合物会发生分解,部分产物转化为尖晶石结构的MgxAlyOz,晶体结构如图2所示,它的化学式为___________;A块、B块均为边长为apm的立方体,设阿伏加德罗常数为NA,则最近的两个Al离子之间的距离为___________pm,密度为___________gcm-3(列出计算表达式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.2-丁烯不存在顺反异构体
B.已知丙烷的二氯代物有四种异构体,则其六氯代物的异构体数目为六种
C.菲的结构简式为 ,它与硝酸反应,可生成4种一硝基取代物
,它与硝酸反应,可生成4种一硝基取代物
D.乙醛的核磁共振氢谱中有二个峰,峰面积之比是1:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com