
| A、电解熔融CeO2制Ce,铈在阳极获得 | ||||||||
B、铈有四种稳定的核素
| ||||||||
| C、用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+ | ||||||||
| D、由于氧化性:Ce4+>Fe3+,而I-有强还原性,所以铈溶于氢碘酸的化学方程式可表示为:2Ce+6HI=2CeI3+3H2↑ |
136 58 |
138 58 |
140 58 |
142 58 |


科目:高中化学 来源: 题型:
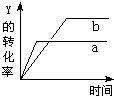 反应 X(气)+Y(气)?2Z(气)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )
反应 X(气)+Y(气)?2Z(气)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )| A、加入催化剂 | B、降低温度 |
| C、增大压强 | D、增大Y的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、d/400 mol/L |
| B、20/d mol/L |
| C、2.5d mol/L |
| D、1.25d mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在实验室,学生一般无需查阅资料即可用75%的硝酸来配制50mL65%的硝酸溶液 |
| B、实验室在配制FeCl3溶液时,常将FeCl3固体溶于较浓的盐酸中 |
| C、用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol.L-1)通常需要用容量瓶等仪器 |
| D、用PH=1的盐酸配制100mLPH=2的盐酸所需全部玻璃仪器有100mL容量瓶、烧杯、玻璃棒、胶头滴管 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①红色褪去的原因是KMnO4将SCN-氧化,使[Fe(SCN)]2+消失 |
| B、②红色褪去的原因是SO2将Fe3+还原为Fe2+ |
| C、②红色褪去的原因是SO2将SCN-还原 |
| D、SCN-在适当条件下可失去电子被氧化剂氧化为(SCN)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放电时负极区溶液的pH逐渐变大 |
| B、K2Zn(OH)4是还原产物,Ag是氧化产物 |
| C、每生成1 mol K2Zn(OH)4 转移 2 mol 电子 |
| D、该电池正极反应式为:Ag2O2+2 e-+2H2O=2Ag+4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 按如图所示装置进行实验,并回答下列问题:
按如图所示装置进行实验,并回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com