
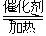 CO2£Øg£©+H2£Øg£©ĪŖĄżĄ“·ÖĪö»ÆŃ§Ę½ŗāµÄ½ØĮ¢”£ŌŚŅ»¶ØĢõ¼žĻĀ£¬½«0.01molCOĘųĢåŗĶ0.01molH2O£Øg£©ĶØČė1LĆܱÕČŻĘ÷ÖŠ£¬æŖŹ¼·“Ó¦”£
CO2£Øg£©+H2£Øg£©ĪŖĄżĄ“·ÖĪö»ÆŃ§Ę½ŗāµÄ½ØĮ¢”£ŌŚŅ»¶ØĢõ¼žĻĀ£¬½«0.01molCOĘųĢåŗĶ0.01molH2O£Øg£©ĶØČė1LĆܱÕČŻĘ÷ÖŠ£¬æŖŹ¼·“Ó¦”£
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 £Ø2013?Ģ©°²Ņ»Ä££©ŃŠ¾æĢ¼¼°Ęä»ÆŗĻĪļµÄŠŌÖŹ¶Ō“Ł½ųµĶĢ¼Éē»įµÄ¹¹½Ø¾ßÓŠÖŲŅŖŅāŅ壮
£Ø2013?Ģ©°²Ņ»Ä££©ŃŠ¾æĢ¼¼°Ęä»ÆŗĻĪļµÄŠŌÖŹ¶Ō“Ł½ųµĶĢ¼Éē»įµÄ¹¹½Ø¾ßÓŠÖŲŅŖŅāŅ壮| ŹµŃé×é | ĪĀ¶Č”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāĖłŠčŹ±¼ä/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ŹµŃé×é | ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāĖłŠčŹ±¼ä/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 6 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 CO2£Øg£©+H2£Øg£©µÄKc=2.6£¬µ±CO£Øg£©ÓėH2O£Øg£©µÄÅØ¶Č£Ømol?L-1£©ŅŌŗĪÖֱȥż£ØÓėĻĀĮŠø÷×鏿¾Ż½Ó½üµÄ£©»ģŗĻŹ±£¬æɵƵ½90%µÄCOµÄ×Ŗ»ÆĀŹ£Ø””””£©
CO2£Øg£©+H2£Øg£©µÄKc=2.6£¬µ±CO£Øg£©ÓėH2O£Øg£©µÄÅØ¶Č£Ømol?L-1£©ŅŌŗĪÖֱȥż£ØÓėĻĀĮŠø÷×鏿¾Ż½Ó½üµÄ£©»ģŗĻŹ±£¬æɵƵ½90%µÄCOµÄ×Ŗ»ÆĀŹ£Ø””””£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| 1 |
| 2 |
| 1 |
| 2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com