
【题目】配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一缺电子的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(缺电子)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是________。
A.CO2 B.H3O+ C.CH4 D.H2SO4
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式:___________________。
(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初,科学家提出了种观点:
甲: 、乙:HOOH,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;c.将生成的A与H2反应(已知该反应中H2做还原剂)。
、乙:HOOH,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;c.将生成的A与H2反应(已知该反应中H2做还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)_____________________________________________________________。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案__________________________________________________________。
【答案】 BD H3BO3+H2O![]() H++[B(OH)4]-
H++[B(OH)4]- 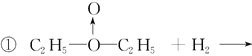
![]() 用无水硫酸铜检验c的反应产物中有没有水(或其他合理答案)
用无水硫酸铜检验c的反应产物中有没有水(或其他合理答案)
【解析】(1)H3O+中O提供孤电子对,H+提供空轨道,NH4+中N提供孤电子对,H+提供空轨道,二者都能形成配位键,答案选BD;(2)硼原子为缺电子原子,H3BO3的电离是B原子和水电离的OH-形成配位键,水电离的H+表现酸性,反应的离子方程式为H3BO3+H2O![]() H++[B(OH)4]-;(3)①如果H2O2的结构如甲所示,实验c中A为
H++[B(OH)4]-;(3)①如果H2O2的结构如甲所示,实验c中A为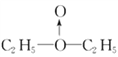 ,与氢气反应生成乙醚,方程式为
,与氢气反应生成乙醚,方程式为![]() C2H5OC2H5+H2O;②如为HO-OH结构,则A为C2H5-O-O-C2H5,与氢气反应生成乙醇,所以可用用无水硫酸铜检验c的反应产物中有没有水生成,如硫酸铜不变蓝,说明没有水生成,则说明过氧化氢中不含配位键,否则含有配位键。
C2H5OC2H5+H2O;②如为HO-OH结构,则A为C2H5-O-O-C2H5,与氢气反应生成乙醇,所以可用用无水硫酸铜检验c的反应产物中有没有水生成,如硫酸铜不变蓝,说明没有水生成,则说明过氧化氢中不含配位键,否则含有配位键。


科目:高中化学 来源: 题型:
【题目】在溶液中能大量共存的一组离子或分子是( )
A. NH4+、H+、NO3-、Fe2+ B. K+ 、Al3+、SO42-- 、NH3·H2O
C. Na+、K+、SO32-、Cl2 D. Na+ 、Cl-、CO32-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时在10 mL 0.1mol·L—1Na2CO3溶液中逐滴加入0.1 mol·L—1HCl溶液20 mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示。下列说法不正确的是

A.HCl溶液滴加一半时,溶液pH>7
B.当溶液的pH=8时,溶液中NaHCO3的物质的量浓度为0.1mol·L—1
C.0.1 mol·L—1Na2CO3溶液中c(Na+)+c(H+)=c(OH—)+2c(CO32—)+c(HCO3—)
D.在M点:c(Na+)>c(CO32—)=c(HCO3—)>c(OH—)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在FeCl3和CuCl2混合液中,加入过量的铁粉,充分反应后,溶液中的金属离子
A. Fe2+ B. Fe3+ 和Fe2+ C. Cu2+ 和Fe2+ D. Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置_________(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置_______。
(2)从碘水中分离出I2,选择装置_______,该分离方法的名称为___________。
(3)装置A中①的名称是_________,进水的方向是从______口进水。装置B在分液时为使液体顺利下滴,应进行的具体操作是______________。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
![]()
粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液; ③加入过量的NaOH溶液; ④调节溶液的pH等于7;⑤溶解; ⑥过滤; ⑦蒸发。正确的操作顺序是__________(填写序号)。
a. ⑤②③①⑥④⑦ b. ⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d. ⑤③②①⑥④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列五种物质 A.阿司匹林 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素, 请按下列要求填空 (填代号):
(1)富含维生素 C 的是 ________;
(2)可直接进入血液,补充能量的是________;
(3)具有消炎作用的是________具有解热镇痛作用的治感冒药是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面合成路线中的化合物I是一种重要的工业原料,用途广泛。

已知:
①烃A的相对分子质量为26。
②化合物B生成化合物C的反应原子利用率100﹪。
③烃E是常用的有机溶剂。
冋答下列问题:
(1)A的化学名称为______________。E分子中共平面的原子数为__________个。
(2)D中的官能团名称是________________。
(3)由B生成C的化学方程式为__________________________。
(4)由E生成F的反应类型为___________;D和H的反应的类型为___________。
(5)同时符合下列条件的G的同分异构体共有____种,任写其中一种的结构简式_____
①能与NaHCO3溶液反应产生气体
②能发生水解反应,且能发生银镜反应
ClCH2COOH是合成甘氨酸的原料之一,现用B物质经两步反应制备ClCH2COOH,合成路线为______________________。(无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电导率是衡量电解质溶液导电能力大小的物理量。常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随加入水的体积V(H2O)变化的曲线如下图所示。下列说法正确的是

A. 曲线I表示NaoH溶液加水稀释过程中溶液电导率的变化
B. a、b、c三点溶液的pH: b>c>a
C. 将a、b两点溶液混合,所得溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH)
D. 醋酸溶液稀释过程中,c(CH3COO-)/c(CH3COOH)不断增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com