
| A. | 2Na2O2+2 Mn2O7=4Na2MnO4+O2 | B. | Na2O2+2NO2=2NaNO2+O2 | ||
| C. | 2Na2O2+2N2O3=4NaNO2+O2 | D. | 2Na2O2+2N2O4=4NaNO3 |
分析 题给信息为:Na2O2可与某些元素的最高价氧化物反应,生成对应的盐(或碱)和O2,Na2O2具有强氧化性,与所含元素不是最高价态的氧化物反应时,只生成相对应的盐,不生成O2,以此解答该题.
解答 解:A.锰的最高价是+7价,应该生成高锰酸钠,故A错误;
B.二氧化氮中的氮不是最高价,所以不产生氧气,应生成硝酸钠,故B错误;
C.N2O3中的氮也不是最高价,所以不产生氧气,不符合上述规律,故C错误;
D.N2O4中N元素为+4价,被氧化生成+5价,生成硝酸钠,不生成氧气,故D正确.
故选D.
点评 本题考查化学反应规律的探究,题目难度中等,注意题中信息:Na2O2可与某些元素的最高价氧化物反应,生成对应的盐(或碱)和O2.


科目:高中化学 来源: 题型:解答题
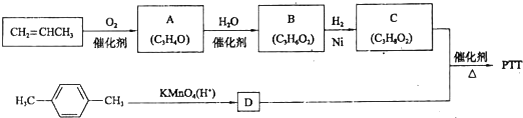
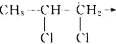
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100gKHCO3和CaCO3的混合物,含有的阳离子数目为NA | |
| B. | 常温常压下,1 mol甲醇完全燃烧生成CO2和H2O,转移的电子数目为6NA | |
| C. | 标准状况下,22.4L丙烷含有的共价键数目为10NA | |
| D. | 常温下,0.1L0.1mol/L的NH4Cl溶液中,NH4+的数目为0.01NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 如下图的转化关系中,已知A是由短周期元素组成的酸式盐.D、Y、H为气体,X为无色液体,G和K均是常见的强酸.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子.
如下图的转化关系中,已知A是由短周期元素组成的酸式盐.D、Y、H为气体,X为无色液体,G和K均是常见的强酸.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
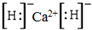 ;这种离子化合物可与水反应,化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑.
;这种离子化合物可与水反应,化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
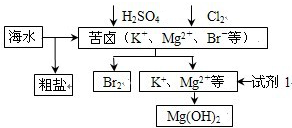
| A. | 试剂1可以选用石灰乳 | |
| B. | 从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2=2 Cl-+Br2 | |
| C. | 工业上,电解熔融MgO冶炼金属镁可减小能耗 | |
| D. | 粗盐经提纯后可用于制备氯气、钠等产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的H2SO4溶液,含H+的数目为2NA | |
| B. | 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 | |
| C. | 273K,101kPa下,14g乙烯与丙烯混合物中含有碳原子数目为3NA | |
| D. | 0.2mol C2H6O分子中一定存在0.2NA个碳碳单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
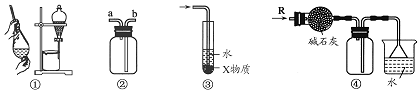
| A. | 装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 | |
| B. | 装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 | |
| C. | 装置①可用于分离C2H5OH和H2O的混合物 | |
| D. | 装置④可用于干燥、收集NH3,并吸收多余的NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com