
����Ŀ��0.2 mol�л����0.55 mol O2���ܱ�������ȼ�պ�IJ���ΪCO2��CO��H2O��g�������ᆳ��Ũ�����Ũ�������������10.8 g����ͨ������CuO��ַ�Ӧ������������4.8 g�����������ͨ����ʯ�ұ���ȫ���գ���ʯ����������26.4 g��
��1��ȼ�պ����CO�����ʵ���___________mol��
��2�����л���ķ���ʽ_____________��
��3�������л�������̼���Ʒ�Ӧ����д�����л���Ľṹ��ʽ___________��
��4�������л������������ˮ�⣬Ҳ�ܷ���������Ӧ������Ϊ____________��
��5���ܷ���������Ӧ������������Ʋ�����������ͬ���칹�干��______�֡�
���𰸡� 0.3 C3H6O2 CH3CH2C OOH �������� 2
����������1������ͨ������CuO������CuO+CO![]() Cu+CO2����ʱ������������4.8 g���ӷ�Ӧ����ʽ��֪��ÿ1molCO��ʹ�ù����ʼ���16g����n(CO)=
Cu+CO2����ʱ������������4.8 g���ӷ�Ӧ����ʽ��֪��ÿ1molCO��ʹ�ù����ʼ���16g����n(CO)= ![]() ��
��
�ʴ�Ϊ��0.3��
��2��Ũ�������������10.8gΪ�л���ȼ������ˮ��������n(H2O)=0.6mol����0.2mol�л����к���n(H)=1.2mol��ÿ�������к���6��Hԭ�ӣ��л���ȼ�����ɵ�CO2��CO��CuO��Ӧ���ɵ�CO2������ʯ����ȫ���գ���ʯ����������26.4gΪCO2��������n(CO2)��=0.6mol�����л���ÿ�������к���3��Cԭ�ӣ��ɣ�1���ʿ�֪��CO��CuO��Ӧ���ɵ�CO2Ϊ0.3mol�����л���ȼ��ʱ����CO2Ϊ0.3mol�����л���ķ���ʽΪC3H6Oz���������������ɵã�
0.2 C3H6Oz + 0.55 O2��0.3 CO2+0.3CO+0.6 H2O������ԭ���غ��֪��
0.2z+0.55��2=0.1��3+0.3��1+0.6��1��z=2�����л���ķ���ʽΪC3H6O2��
�ʴ�Ϊ��C3H6O2��
��3��C3 H6 O2��Hԭ�ӱ�C3 H8��2��H�������Ͷ�Ϊ1�������л�������̼���Ʒ�Ӧ��������к���1��-COOH���÷���Ϊ���ᣬ�ṹ��ʽΪ��CH3CH2COOH��
�ʴ�Ϊ��CH3CH2COOH��
��4������������ˮ����Ӧ�����������ܷ���������Ӧ��Ӧ��ȩ�����ַ��ӵIJ����Ͷ�Ϊ1����Ӧ���Ǽ����������ṹ��ʽΪ��HCOOCH2CH3����Ϊ����������
�ʴ�Ϊ������������
��5���ܷ���������Ӧ��Ӧ��ȩ������������Ʋ�������Ӧ���ǻ��������ķ��������֣�HOCH2CH2CHO��CH3CHOHCHO��
�ʴ�Ϊ��2.


 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ƣ�Na2S2O5���dz��õĿ����������ڿ����С�����ʱ���ֽ⣮ʵ�����Ʊ�����Na2S2O5�ķ������ڲ��Ͻ����£����Ʒ�Ӧ�¶���40�����ң���Na2CO3��������Һ��ͨ��SO2 �� ʵ��װ����ͼ��ʾ�� 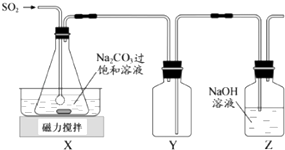
����ҺpHԼΪ4ʱ��ֹͣ��Ӧ����20�����Ҿ��ýᾧ������Na2S2O5�Ļ�ѧ����ʽΪ��2NaHSO3�TNa2S2O5+H2O
��1��SO2��Na2CO3��Һ��Ӧ����NaHSO3��CO2 �� �����ӷ���ʽΪ ��
��2��װ��Y��������
��3����������ķ�ӦҺ����ѹ���ˡ�ϴ�ӡ�25�橁30�����ɻ��Na2S2O5���壮
����ɼ�ѹ����װ�õ���Ҫ�����Dz���©�����ͳ����ã�
�������ñ���SO2ˮ��Һ����ˮ�Ҵ�ϴ��Na2S2O5���壮�ñ���SO2ˮ��Һϴ�ӵ�Ŀ���� ��
��4��ʵ���Ƶõ�Na2S2O5�����к���һ������Na2SO3��Na2SO4 �� ����ܵ�ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����������Һ�мȿ��Դ������棬�Ҽ��������ˮ��Ҳ��������������
A.K�� AlO2�� NO3�� OH��B.���� NH4�� Al3�� SO42��
C.Na�� Ba2�� Cl�� SO42��D.H�� Cl�� CH3COO�� NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ���Ԫ��������������ȷ���ǣ� ��
A.����Ԫ�ص�ԭ��ֻ�л�ԭ�ԣ�����ֻ��������
B.����Ԫ�صĵ����ڳ����¾�Ϊ��������
C.����Ԫ���ڲ�ͬ�Ļ������еĻ��ϼ۾���ͬ
D.����Ԫ����һ�㻯������ֻ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(2017�����Ͼ�)����ʵ�������ȷ����
A���ζ�ǰ�ô���Һ��ϴ��ƿ
B������ƿ�͵ζ���ʹ��ǰ����Ҫ��©
C���������ʱ���ȹر�����ˮ����ֹͣ����
D����Һʱ���²���Һ�ȴ��¿ڷų����ϲ���Һ�ٴ��Ͽڵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʵ��л���������ͬ���칹����Ŀ�����ǣ������������칹����������
ѡ�� | A | B | C | D |
����ʽ | C4H8Cl2 | C5H10O2 | C4H8O2 | C9H12 |
��� | ���Ȼ����� | ���� | �� | ���б������� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.6molX�����0.4mol Y��������2L�����У�������Ӧ��3X��g��+Y��g���TnZ��g��+2W��g����5minĩ������0.2mol W������֪��ZŨ�ȱ仯����ʾ��ƽ������Ϊ 0.03molL��1min��1 �� ���㣺
��1��n��ֵΪ
��2��ǰ5min����X��ʾ�ķ�Ӧ����
��3��5minĩY��Ũ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ù���NaOH����һ�����ʵ���Ũ�ȵ���Һʱ�����в����ᵼ����ҺŨ��ƫ������
A. ���ձ����ܽ�ʱ��������Һ�彦��
B. ����ʱ��������ƿ�̶���
C. ����ƿʹ��ǰδ����
D. δ��ȴ�����½���Һת�Ƶ�����ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ʷ����˵����ȷ����
A.��֬�����ࡢ�����ʾ�����Ȼ�߷��ӻ�����
B.���ȼ��顢����ϩ�����屽�Ӿ���±����
C.CaCl2���ռ�۱���ϩ��Ϊ������
D.ϡ���������ᡢ������Ϊ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com