
高锰酸钾是一种典型的强氧化剂。
完成下列填空:
Ⅰ.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①MnO +Cu2S+H+―→Cu2++SO2↑+Mn2++H2O(未配平)
+Cu2S+H+―→Cu2++SO2↑+Mn2++H2O(未配平)
②MnO +CuS+H+―→Cu2++SO2↑+Mn2++H2O(未配平)
+CuS+H+―→Cu2++SO2↑+Mn2++H2O(未配平)
(1)下列关于反应①的说法中错误的是________(填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
(2)标出反应②中电子转移的方向和数目:MnO +CuS
+CuS
Ⅱ.在稀硫酸中,MnO 和H2O2也能发生氧化还原反应
和H2O2也能发生氧化还原反应
氧化反应:H2O2-2e-===2H++O2↑
还原反应:MnO +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
(3)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为________。由上述反应得出的物质氧化性强弱的结论是________>________(填写化学式)。
(4)已知:2KMnO4+7H2O2+3H2SO4===K2SO4+2MnSO4+6O2↑+10H2O,则被1 mol KMnO4氧化的H2O2是________ mol。
答案 (1)d (2)6MnO +5CuS30e-
+5CuS30e-
(3)6.02×1023 KMnO4>H2O2(或O2) (4)2.5
解析 (1)①中,a项铜元素的化合价由+1升到+2价,硫元素的化合价由-2升到+4价,均被氧化,正确;b项,设氧化剂的物质的量为x,还原剂的物质的量为y,则5x=(2+6)y, =
= ,正确;c项,根据b项,当生成5 mol SO2时,转移电子40 mol,所以当有0.1 mol SO2生成时,转移电子0.8 mol,正确;d项,根据方程式,还原性Cu2S>Mn2+,错误。(2)由②可得,锰元素化合价由+7降到+2,硫元素化合价由-2升到+4,根据得失电子守恒得6MnO
,正确;c项,根据b项,当生成5 mol SO2时,转移电子40 mol,所以当有0.1 mol SO2生成时,转移电子0.8 mol,正确;d项,根据方程式,还原性Cu2S>Mn2+,错误。(2)由②可得,锰元素化合价由+7降到+2,硫元素化合价由-2升到+4,根据得失电子守恒得6MnO +5CuS30e-。(3)由H2O2-2e-===2H++O2↑得,当有0.5 mol H2O2参加此反应,转移电子个数为NA,在该反应中,MnO
+5CuS30e-。(3)由H2O2-2e-===2H++O2↑得,当有0.5 mol H2O2参加此反应,转移电子个数为NA,在该反应中,MnO 是氧化剂,H2O2是还原剂,所以,氧化性KMnO4>O2(或H2O2)。(4)方程式可改写成2KMnO4+5H2O2+3H2SO4===K2SO4+2MnSO4+5O2↑+8H2O
是氧化剂,H2O2是还原剂,所以,氧化性KMnO4>O2(或H2O2)。(4)方程式可改写成2KMnO4+5H2O2+3H2SO4===K2SO4+2MnSO4+5O2↑+8H2O
2H2O2===2H2O+O2↑, 所以被1 mol KMnO4氧化的H2O2是2.5 mol。
所以被1 mol KMnO4氧化的H2O2是2.5 mol。


科目:高中化学 来源: 题型:
下列变化过程中表示的能量转化关系错误的是 ( )
A.植物光合作用:光能→生物质能 B.木柴烧饭:生物质能→热能
C.电灯发光:电能→化学能 D.太阳能热水器:光能→热能
查看答案和解析>>
科目:高中化学 来源: 题型:
铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生: ①Tl3++2Ag===Tl++2Ag+,②Ag++Fe2+===Ag+Fe3+,③Fe+2Fe3+===3Fe2+,下列离子氧化性比较顺序正确的是 ( )
A.Tl3+>Fe3+>Ag+ B.Fe3+>Ag+>Tl3+
C.Tl+>Ag+>Fe2+ D.Tl3+>Ag+>Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原
B.元素由化合态变成游离态时,它可能被氧化,也可能被还原
C.失电子难的原子,获得电子的能力一定强
D.有单质参加或生成的反应一定属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4===2NaHSO4+MnSO4+2H2O+I2;②2NaIO3+5NaHSO3===2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是 ( )
A.两个反应中均为硫元素被氧化
B.碘元素在反应①中被还原,在反应②中被氧化
C.氧化性:MnO2>SO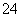 >IO
>IO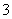 >I2
>I2
D.反应①、②中生成等量的I2时转移电子数之比为1∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是( )。
A.FeCl3溶液与Cu的反应:Fe3++Cu=Cu2++Fe2+
B.NO2与水的反应:3NO2+H2O=2NO3-+NO+2H+
C.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑
D.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO3 2-
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数的值,下列说法中正确的是( )。
A、84gNaHCO3晶体中含有NA个CO32-
B、9.2gNO2和N2O4的混合气体中含有的氮原子数为0.2NA
C、标准状况下,11.2L臭氧中含NA个氧原子
D.标准状况下,由Na2O2制得11.2 L O2,反应转移的电子数为0.5 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com