
【题目】铝、铁是常见的两种金属,它们的单质及化合物在生活生产中处处可见。
(1)过量的铁和稀硝酸发生反应,产物是Fe(NO3)2和NO,写出该反应的化学方程式___________。
(2)实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为_______(填写化学式)。在该溶液中加入___________试剂,看到_____________________现象,证明溶液变质。
(3)KAl(SO4)2·12H2O俗称明矾,常用作净水剂,请述其原因并写出有关的离子方程式____________________。
(4)已知Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。
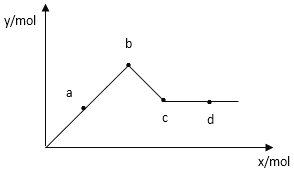
由图可知c点的沉淀是________(填化学式),已知a-b时存在的沉淀是Al(OH)3和BaSO4,两者的物质的量:________比________多。
【答案】 3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O Fe2(SO4)3 KSCN溶液 溶液变为血红色 明矾水解生成胶状Al(OH)3,它具有很强的吸附能力,可以吸附水中的杂质并沉降,使水澄清。Al3++3H2O![]() Al(OH)3+3H+ BaSO4 BaSO4 Al(OH)3
Al(OH)3+3H+ BaSO4 BaSO4 Al(OH)3
【解析】(1)过量的铁和稀硝酸发生反应,产物是Fe(NO3)2和NO,反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O;(2)实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为Fe2(SO4)3。在该溶液中加入KSCN溶液,溶液变为血红色,证明溶液变质;(3)KAl(SO4)2·12H2O俗称明矾,明矾水解生成胶状Al(OH)3,它具有很强的吸附能力,可以吸附水中的杂质并沉降,使水澄清,常用作净水剂,有关的离子方程式为Al3++3H2O![]() Al(OH)3+3H+;c点时Al(OH)3沉淀恰好完全溶解,此时产生的沉淀只有BaSO4;在a-b发生反应A12(SO4)3+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓,由方程式可知,沉淀的物质的量: BaSO4比Al(OH)3多。
Al(OH)3+3H+;c点时Al(OH)3沉淀恰好完全溶解,此时产生的沉淀只有BaSO4;在a-b发生反应A12(SO4)3+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓,由方程式可知,沉淀的物质的量: BaSO4比Al(OH)3多。


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案科目:高中化学 来源: 题型:
【题目】298 K时,各反应的平衡常数如下:
①N2(g)+O2(g)![]() 2NO(g),K=1×10-30;
2NO(g),K=1×10-30;
②2H2(g)+O2(g)![]() 2H2O(g),K=2×1081;
2H2O(g),K=2×1081;
③2CO2(g)![]() 2CO(g)+O2(g),K=4×10-92
2CO(g)+O2(g),K=4×10-92
则常温下,NO、H2O、CO2这三个化合物分解放氧的倾向最大的是( )
A.① B.② C.③ D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关细胞物质组成的叙述,正确的是
A. 在人体活细胞中氧原子的数目最多
B. 脂肪细胞含量最多的化合物是脂肪
C. 每种细胞所含的有机物最多的都是蛋白质
D. 组成蛋白质的元素一定有C、H、O、N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修3:物质结构与性质】铁、钻、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
(1)基态钴原子的价电子排布式为________,铁、钴、镍的基态原子核外未成对电子数最少的是_____________
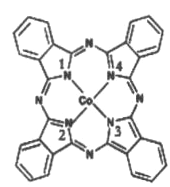
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是__________ (填1、2、3、4),三种非金属原子的电负性由大到小的顺序为____(用相应的元素符号表示);碳原子的杂化轨道类型为_________
(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO) x晶体属于_______ (填晶体类型),若配合物Fe(CO) x的中心原子价电子数与配体提供电子数之和为18,则x=_________
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO ______ FeO(填“>”“<”或“=”),原因是___________________________。
(5)NiAs的晶胞结构如图所示:
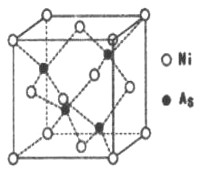
①镍离子的配位数为_________。
②若阿伏加德罗常数的值为NA,晶体密度为pg.cm-1,则该晶胞中最近的离子之间的距离为_____cm。(写出计算表达式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对实验室制取氨气,下列说法不正确的是( )
A.发生装置与用KClO3制取O2的装置相同
B.可用排饱和氯化铵溶液的方法收集氨气
C.氨气的验满可以用湿润的红色石蕊试纸或蘸有浓盐酸的玻璃棒放于试管口附近
D.所用的铵盐不是NH4NO3,是因为NH4NO3受热易爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和反应速率的测定。将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡气体总浓度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
(1)可以判断该分解反应已经达到平衡的是________。
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
E.单位时间内消耗1 molNH2COONH4 ,同时生成2mol NH3
F.密闭容器中混合气体的平均摩尔质量不变 G.容器内NH3与CO2的浓度之比为2∶1 H.6个N—H键断裂的同时,有2个C=O键形成
(2)根据表中数据,计算25.0 ℃时的分解平衡常数______________。
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量________(填“增加”、“减少”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,我国在航空航天事业上取得了令人瞩目的成就,科学家在能量的转化,航天器的零排放作出了很大的努力,其中为了达到零排放的要求,循环利用人体呼出的CO2并提供O2,设计了一种装置(如图)实现了能量的转化。总反应方程式为2CO2=2CO+O2。关于该装置下列说法正确的是
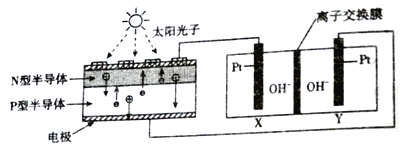
A. 装置中离子交换膜为阳离子交换膜
B. CO2参与X电极的反应方程式:CO2+2e-+H2O=CO+2OH-
C. N型半导体为正极,P型半导体为负极
D. 外电路每转移2mol电子,Y极生成气体22.4L(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面:锂混杂于其中。(已知Co2O3的氧化性>Cl2的氧化性)从废料中回收氧化钴(CoO)的工艺流程如下:
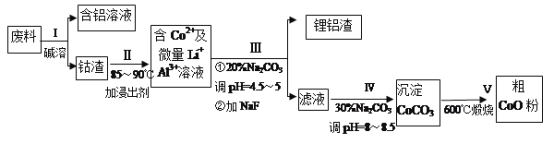
已知:①CoCO3的溶度积为:Ksp=1.0×10-13;
②溶液中离子浓度小于1.0×10-5mol/L时认为该离子沉淀完全。
(1)“碱溶”前通常将废料粉碎,其目的是____________。
(2)过程I中采用NaOH溶液溶出废料中的A1,反应的离子方程式为_________________。
(3)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出含钻物质的反应化学方程式为 (产物中只有一种酸根) _______________________________________。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请分析不用盐酸浸出钴的主要原因______________________________________。
(4)过程III得到锂铝渣的主要成分是LiF和AI(OH)3,碳酸钠溶液在产生 Al(OH)3时起重要作用,请写出该反应的离子方程式__________________________________。
(5)将2.0×10-4 mol/LCoSO4与2.2×10-4mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为__________,Co2+是否沉淀完全? __________(填“是”或“否”)。
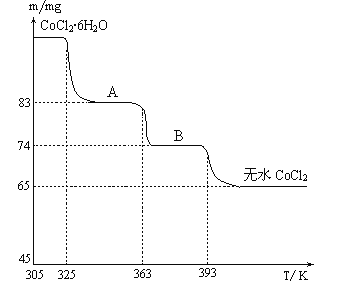
(6)CoO溶于盐酸可得粉红色的CoCl2溶液。CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,物质B的化学式是____________________。
【答案】 略 略 略 略 略 略 略 略
【解析】(1). “碱溶”前通常将废料粉碎,可以增大固体反应物的接触面积,加快反应速率,故答案为:增大反应物接触面积,加快反应速率;
(2). NaOH溶液和Al反应生成偏铝酸钠和氢气,离子方程式为:2A1+2OH-+2H2O=2A1O2-+3H2↑,故答案为:2A1+2OH-+2H2O=2A1O2-+3H2↑;
(3). 废料中钴以Co2O3·CoO的形式存在,钴的化合价为+2价和+3价,由流程图可知,加入Na2S2O3溶液后,钴全部变为+2价,说明Co3+氧化S2O32-,还原产物为Co2+,由产物中只有一种酸根离子可知氧化产物为SO42-,根据得失电子守恒和原子守恒,浸出含钴物质的反应化学方程式为:4Co2O3·CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O,由题中信息可知,Co2O3的氧化性>Cl2的氧化性,则Co2O3·CoO可氧化盐酸产生Cl2,污染环境,所以实际工业生产中不用盐酸浸出含钴物质,故答案为:4Co2O3·CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O;Co2O3·CoO可氧化盐酸产生Cl2,污染环境;
(4). 在过程III中加入碳酸钠溶液,碳酸根离子和铝离子发生双水解反应生成氢氧化铝沉淀,离子方程式为:2A13++3CO32-+3H2O=2A1(OH)3↓+3CO2↑,故答案为:2A13++3CO32-+3H2O=2A1(OH)3↓+3CO2↑;
(5). 将2.0×10-4mol/LCoSO4与2.2×10-4mol/L的Na2CO3等体积混合,Co2+与CO32-反应生成CoCO3,离子方程式为:Co2++ CO32-= CoCO3,由离子方程式可知,反应后的溶液中c(CO32-)=( 2.2×10-4-2.0×10-4)mol/L÷2=1×10-5mol/L,则反应后的溶液中c(Co2+)=![]() =1.0×10-8mol/L,c(Co2+)<1.0×10-5mol/L,所以Co2+沉淀完全,故答案为:1.0×10-8mol/L;是;
=1.0×10-8mol/L,c(Co2+)<1.0×10-5mol/L,所以Co2+沉淀完全,故答案为:1.0×10-8mol/L;是;
(6). 据图可知,n(CoCl2)=65×10-3g÷130g/mol=5×10-4mol,B中含有水的物质的量为n(H2O)=(74-65)×10-3g÷18g/mol=5×10-4mol,则n(CoCl2): n(H2O)=1:1,则物质B为CoCl2·H2O,故答案为:CoCl2·H2O。
【题型】综span>合题
【结束】
10
【题目】砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
(1)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图1写出As2O3转化为As2O5的热化学方程式__________________________________。
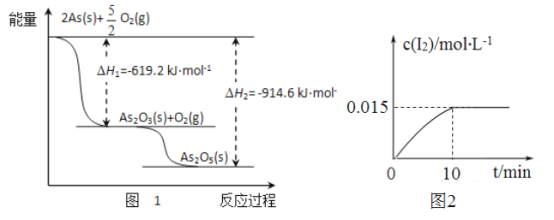
(2)砷酸钠具有氧化性,298K时,在100mL烧杯中加入10mL0.1 mol/L Na3AsO4溶液、20mL0.1 mol/L KI溶液和20mL0.05mol/L硫酸溶液,发生下列反应:AsO43-(无色)+12(浅黄色)+H2O △H。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
①升高温度,溶液中AsO43-的平衡转化率减小,则该反应的△H________0(填“大于”“小于”或“等于”)。
②0~10min内,I的反应速率v(Iˉ)= ____________。
③下列情况表明上述可逆反应达到平衡状态的是_______(填字母代号)。
a.c(AsO33-)+c(AsO42-)不再变化 b.溶液颜色保持不再变化
C.c(AsO33-)与c(AsO42-)的比值保持不再变化 d.I的生成速率等于I2的生成速率
④在该条件下,上述反应平衡常数的表达式K=______________。
(3)利用(2)中反应可测定含As2O3和As2O5的试样中的各组分含量(所含杂质对测定无影响),过程如下:
①将试样02000g溶于NaOH溶液,得到含AO33-和AsO43-的混合溶液。
②上述混合液用0.02500 mol·L-1的I2溶液滴定,用淀粉试液做指示剂,当________________,则滴定达到终点。重复滴定3次,平均消耗I2溶液40.00mL。则试样中As2O5的质量分数是_________(保留四位有效数字)。若滴定终点时,仰视读数,则所测结果_________ (填“偏低”,“偏高”,“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化合物的说法正确的是
A. 干冰的主要成分是H2O B. 吸入CO可导致人体中毒
C. SO2可大量用于漂白食品 D. 小苏打的主要成份是Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com