
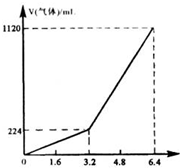
 ��һ������Ͼ��ȵ�����������ڸ��������������¹��ȣ���ַ�Ӧ����ȴ�����£��õ�����A��������Ϊm�Ĺ���A���뵽300mL 2mol/L������ʹ֮��ȫ�ܽ⣮��������¼������A���������ռ�������������ѻ���ɱ�״�����Ĺ�ϵ��ͼ��ʾ������������������Һ����ǰ�����������ݳ�������֪���ټ������A������m��3.2gʱ���ռ���������ΪH2���ڵ�m��3.2gʱ���ռ���������ΪH2��H2S�Ļ�����壮
��һ������Ͼ��ȵ�����������ڸ��������������¹��ȣ���ַ�Ӧ����ȴ�����£��õ�����A��������Ϊm�Ĺ���A���뵽300mL 2mol/L������ʹ֮��ȫ�ܽ⣮��������¼������A���������ռ�������������ѻ���ɱ�״�����Ĺ�ϵ��ͼ��ʾ������������������Һ����ǰ�����������ݳ�������֪���ټ������A������m��3.2gʱ���ռ���������ΪH2���ڵ�m��3.2gʱ���ռ���������ΪH2��H2S�Ļ�����壮���� ��1����������ڼ���ʱ���ܹ��������������Ӧ��
��2�����ݡ���m��3.2gʱ���ռ���������ΪH2��H2S����֪��Ӧ�����ΪFeS��Fe��������Ӧ�У�������Ӧ�����Ȼ��������Ȼ����������ᷴӦ�����Ȼ��������Ȼ��⣬����ϡ���ᷴӦ�����Ȼ��������������ݴ�д����Ӧ�ķ���ʽ��
��3������������ڸ������������¹��Ⱥ������ɵIJ���������������������һ��FeS��S������FeS��Fe������FeS��������뵽300 mL 2 mol•L-1�������ܹ���ȫ�ܽ⣬�����A�в����ڵ������ų��˵�һ�����������m��3.2 gʱ�ռ�������ΪH2��H2S�Ļ�������ɵó�����A��FeS��Fe�Ļ���������ͼ��֪�ڹ���A������m��3.2 gʱ���ռ���������ֻ��H2����ǰ�����ɵ�H2Sȫ������ˮ�У�Ҳ����m=3.2 gʱ��H2S��ˮ�е��ܽ�ﵽ����״̬������Fe��H2�ɼ����������������������FeS������������n=$\frac{m}{M}$����������ʵ���������H2S�����ʵ���Ϊn��H2S��=n��FeS��������c=$\frac{n}{V}$����������ʵ���Ũ�ȣ�
��4����m=3.2 gʱ��H2S��ˮ�е��ܽ�ﵽ���ͣ���m��3.2 gʱ����H2Sˮ��Һ�Ѿ����ͣ���ʱ�����H2S��������ɹ�ϵʽ��Fe��H2��FeS��H2S�������غ�֪������A�Ͳ�����������ʵ���֮��Ϊ1��1���ݴ˽�ϣ�2�������ݼ���mg����ɲ���H2��H2S���������ȥ�ܽ�����������Ϊ�ռ�����������
��� �⣺��1��Ϊ�˱���Fe��S�ڼ�����������������Ӧ���÷�Ӧ��Ҫ�ڸ��������������½��У�
�ʴ�Ϊ���������ۡ������������Ӧ��
��2����m��3.2gʱ���ռ���������ΪH2��H2S����Ӧ�����ΪFeS��Fe��������Ӧ�У�������Ӧ�����Ȼ�������Fe+S$\frac{\underline{\;\;��\;\;}}{\;}$FeS���Ȼ����������ᷴӦ�����Ȼ��������Ȼ��⣺FeS+2HCl=H2S+FeCl2������ϡ���ᷴӦ�����Ȼ�������������Fe+2HCl=FeCl2+H2����
�ʴ�Ϊ��Fe+S$\frac{\underline{\;\;��\;\;}}{\;}$FeS��FeS+2HCl=H2S+FeCl2��Fe+2HCl=FeCl2+H2����
��3������������ڸ������������¹��Ⱥ������ɵIJ���������������������һ��FeS��S������FeS��Fe������FeS�������⣬������뵽300 mL 2 mol•L-1�������ܹ���ȫ�ܽ⣬�ɵù���A�в����ڵ������ų��˵�һ��������������m��3.2 gʱ���ռ�������ΪH2��H2S�Ļ�������ɵó�����A��FeS��Fe�Ļ���
������ͼ��֪�ڹ���A������m��3.2 gʱ���ռ���������ֻ��H2����ǰ�����ɵ�H2Sȫ������ˮ�У�Ҳ����m=3.2 gʱ��H2S��ˮ�е��ܽ�ﵽ����״̬��n��H2��=$\frac{0.224L}{22.4L/mol}$0.01 mol��
��Fe��H2��֪��m��Fe��=0.01 mol��56 g•mol-1=0.56 g
��m��FeS��=3.2 g-0.56 g=2.64 g�����������غ�ɵã�n��FeS��=$\frac{2.64g}{88g/mol}$=0.03 mol��
��������Һ������������ʵ���Ũ��Ϊ��c��H2S��=$\frac{0.03mol}{0.3L}$=0.1 mol•L-1
�ʴ�Ϊ��Fe��FeS��n��Fe��=0.01mol��n��FeS��=0.03mol��0.1mol•L-1��
��4����m=3.2 gʱ��H2S��ˮ�е��ܽ�ﵽ���ͣ���Ӧ�������������������Ϊ224mL+0.03mol��22.4L/mol��1000mL/L=896mL��
��m��3.2 gʱ����H2Sˮ��Һ�Ѿ����ͣ���ʱ�����H2S��������ɹ�ϵʽ��Fe��H2��FeS��H2S�������غ�֪������A�Ͳ�����������ʵ���֮��Ϊ1��1����mg����ɲ���H2��H2S�����Ϊ��$\frac{mg}{3.2g}$��896mL=280m mL��������672 mL��H2S�ܽ�����Һ�У�����ʵ���ռ���������Ϊ����280m-672��mL��
�ʴ�Ϊ����280m-672����
���� ���⿼�����ﷴӦ�ļ��㣬��Ŀ�ѶȽϴ��������Ϣ��ȷ������Ӧԭ��Ϊ���ؼ���ע�������غ㷨�ͼ�ֵ���ڻ�ѧ�����е�Ӧ�ã�������ؿ���ѧ����ʶͼ������������ѧ֪ʶ�����ѧ�����������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����й������������в���ȷ���ǣ�������
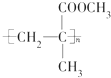
�����й������������в���ȷ���ǣ�������| A�� | 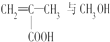 ��һ�������·������۷�Ӧ���ɺϳɸ��л����� ��һ�������·������۷�Ӧ���ɺϳɸ��л����� | |
| B�� | ���л������ܷ���������Ӧ | |
| C�� | �ϳɸ��л�������ԭ�Ͽ����м��� | |
| D�� | ����һ�������·���ˮ�ⷴӦʱC-O������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϵͳ�������������� 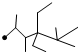 �������� 2��3��5��5-�ļ�-4��4-���һ����� �������� 2��3��5��5-�ļ�-4��4-���һ����� | |
| B�� | �����ʵ����ı��ͱ�������ȫȼ������������������� | |
| C�� | ����ױ���Ϊͬϵ�����ʹKMnO4������Һ��ɫ | |
| D�� | �ṹƬ��Ϊ 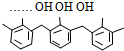 ���ĸ߾���䵥���Ǽ�ȩ�ͱ��� ���ĸ߾���䵥���Ǽ�ȩ�ͱ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
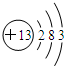 ��
��| Ԫ�� | Na | Mg | Al | Si | P | S | Cl |
| �縺�� | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6.02��1023 ���ǰ���ӵ����� | |
| B�� | 1 Ħ����������2NA����ԭ�� | |
| C�� | 1 Ħ���κ����ʶ�����6.02��1023 ������ | |
| D�� | 1 Ħ��ˮ����18��6.02��1023 ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
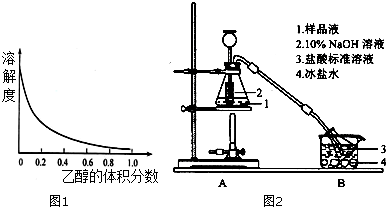
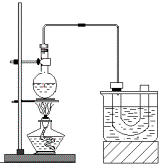 ʵ�����Ʊ������飨C2H5Br����װ�úͲ�����ͼ������֪������ķе�38.4�棩
ʵ�����Ʊ������飨C2H5Br����װ�úͲ�����ͼ������֪������ķе�38.4�棩�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com