
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1 mol/L的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是
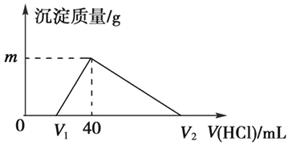
A.原合金质量为 0.92 g B.产生氢气的体积为896 mL(标准状况下)
C.图中m的值为1.56 D.图中V2的值为60
【知识点】有关混合物反应的计算;钠的化学性质;铝的化学性质.C1 C2
【答案解析】C 解析: 由图象可知,向合金溶解后的溶液中加盐酸,
先发生NaOH+HCl═NaCl+H2O,后发生NaAlO2+HCl+H2O═NaCl+Al(OH)3↓,
最后发生Al(OH)3↓+3HCl═AlCl3+3H2O,
合金溶解后剩余的氢氧化钠的物质的量为0.02L×1mol/L=0.02mol,
由NaOH+HCl═NaCl+H2O,
0.02mol 0.02mol
则V1为0.02mol/1mol/L=0.02L=20mL,
生成沉淀时消耗的盐酸为40mL-20mL=20mL,其物质的量为由0.02L×1mol/L=0.02mol,
由 NaAlO2+HCl+H2O═NaCl+Al(OH)3↓,
0.02mol 0.02mol 0.02mol
A、由钠元素及铝元素守恒可知,合金的质量为
0.04mol×23g/mol+0.02mol×27g/mol=1.46g,故A错误;
D、由Al(OH)3↓+3HCl═AlCl3+3H2O可知,溶解沉淀需要0.06molHCl,其体积为60mL,则V2为40mL+60mL=100mL,故D错误
C、由上述计算可知,生成沉淀为0.02mol,其质量为0.02mol×78g/mol=1.56g,正确;
B、由2Na+2H2O═2NaOH+H2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,生成氢气的物质的量为0.02mol+0.03mol=0.05mol,其标况下的体积为0.05mol×22.4L/mol=1.12L,错误.
【思路点拨】本题考查了本题考查钠、铝的化学性质及反应,明确发生的化学反应及反应与图象的对应关系是解答本题的关键,并学会利用元素守恒的方法来解答,综合性较强,难度较大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
1814年戴维发现了一氯化碘(ICl)、三氯化碘(ICl3),由于它们的性质与卤素相似,因此被称为卤素互化物。
(1)氯元素在元素周期表中的位置是_________;ICl的电子式为____________。
(2)ICl与冷的NaOH稀溶液反应的离子方程式为____________________。
(3)用海带制碘时,生成的粗碘中常混有ICl,可加入KI加热升华提纯,发生化学反应的化学方程式为_____________________。
(4)三氯化碘常以二聚体I2Cl6的形式存在,经电导仪测定知,它能发生部分电离,生成的两种离子的相对质量分别为198和269,其电离方程式为_________________________。下列说法正确的是______。
a.ICl3分子中各原子均达到8电子稳定结构
b.由反应KClO3+I2+6HCl=2ICl3+KCl+3H2O,可知还原性:KClO3>ICl3
c.ICl与乙烯反应的化学方程式为CH2=CH2+ICl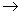 ICH2CH2Cl
ICH2CH2Cl
d.ICl与苯反应制取碘苯的化学方程式为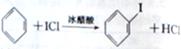
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.下列有关说法不正确的是________。
A.相同类型的离子晶体,晶格能越大,形成的晶体越稳定
B.NH3和H3O+是等电子体,因此结构都是三角锥形
C.邻羟基苯甲醛沸点低于对羟基苯甲醛,原因是前者存在分子内氢键后者存在
分子间氢键
D.H3O+、HF2-和[Ag(NH3)2]+中均存在配位键
Ⅱ.碳及其化合物在自然界中广泛存在。
(1)基态碳原子的价电子排布图可表示为 。第四周期与其有相同
未成对电子数的过渡金属有 (填元素符号)
(2)第一电离能:C、N、O、F四种元素由大到小顺序___ _ ,
原因是 ,
HCN、NF3分子构型分别是 。
(3)冰晶胞中水分子的空间排列方式与金刚石晶胞类似。每个冰晶胞平均占有________个水分子,冰晶胞与金刚石晶胞排列方式相同的原因是__________________________。
(4)C60的晶体中,分子为面心立方堆积,已知晶胞中C60分子中心间的最短距离为
d cm,可计算C60晶体的密度为________g/cm3。
(5)请写出一个反应方程式以表达出反应前碳原子的杂化方式为sp2,反应后变为sp3:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入到FeC12溶液中 ②过量NaOH溶液和明矾溶液馄合 ③少量Ca (OH)2投入过量NaHCO3溶液中 ④向NaAlO2溶液中通入过量CO2 ⑤向饱和Na2CO3溶液中通入过量CO2
A.①②③④⑤ B.只有①④ C.只有②③ D.只有③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
A是自然界存在最广泛的ⅡA族元素,常以化合物F存在。从单质A起始发生的一系列化学反应可由下图表示:
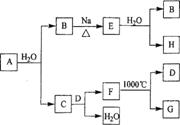
请回答下列问题:
(1)A与水反应的化学方程式为____________,E与水反应的化学方程式为___________;
(2)F的化学式为_____________,G和D的电子式分别为____________和______________;
(3)D与H反应可能生成的盐有_______________ (填化学式);
(4)如何由F制备A : 。
查看答案和解析>>
科目:高中化学 来源: 题型:
.类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中,错误的是
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③化合物NaCl的焰色为黄色;Na2CO3的焰色也为黄色
④密度为1.1 g·cm-3与密度为1.2 g·cm-3的NaCl溶液等体积混合,所得NaCl溶液的密度介于1.1 g·cm-3与1.2 g·cm-3之间,Na-K合金的熔点应介于Na和K熔点之间
A.①② B.①④ C.①②③④ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
.下列关于金属钠的叙述错误的是
A.金属钠可以保存在煤油中
B.金属钠着火时,可用泡沫灭火器来灭火
C.钠与熔融的四氯化钛反应可制取钛
D.实验时用剩的钠块应该放回原试剂瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| 化学式 | 电离常数 |
| HClO | K=3×10-8 mol·L-1 |
| H2CO3 | K1=4.3×10-7 mol·L-1 |
| K2=5.6×10-11 mol·L-1 |
A.[HCO ]>[ClO-]>[OH-]
]>[ClO-]>[OH-]
B.[ClO-]>[HCO ]>[H+]
]>[H+]
C.[HClO]+[ClO-]=[HCO ]+[H2CO3]
]+[H2CO3]
D.[Na+]+[H+]=[HCO ]+[ClO-]+[OH-]
]+[ClO-]+[OH-]
查看答案和解析>>
科目:高中化学 来源: 题型:
以下判断,结论正确的是
| 选项 | 项目 | 结论 |
| A | 三种有机化合物:丙烯、氯乙烯、苯 | 分子内所有原子均在同一平面 |
| B | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | 属于同一反应类型 |
| C | 乙烯和苯都能使溴水褪色 | 褪色的原理相同 |
| D | C4H9Cl的同分异构体数目(不考虑立体异构) | 共有4种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com