

分析 (1)根据题目的信息有极强的还原性.受热、遇水都会发生分解反应放出大量的热,甚至引起燃烧,所以保险粉要密封、阴凉处保存;
(2)①SO2中的硫+4价,而Na2S2O4中的硫+3价,所以硫的化合价降低,所以二氧化硫表现为氧化性;实验室用浓度较大的硫酸和亚硫酸盐反应,生成二氧化硫,盐酸易挥发,而稀硫酸溶液中水太多,大多数SO2生成了亚硫酸,不生成SO2气体,因为SO2易溶于水,1个体积的水溶解40个体积的SO2,硝酸有强氧化性;
②Ksp=c(Zn2+)•c2(OH-)来计算氢氧根离子浓度,然后根据水的离子积常数计算pH;
③因为Na2S2O4易溶于水,但不溶于乙醇,所以可以用乙醇来洗涤沉淀;
(3)根据反应硫的化合价+4价,而Na2S2O4中的硫+3价,化合价降价,根据电子得失守恒,HCOONa中的碳的化合价必然升高,由+2价变成+4价,然后由质量守恒定进行分析;
(4)反应①与反应②中都生成亚硫酸氢钠,而反应②中还产生硫酸氢钠,硫酸氢钠在水溶液中完全电离产生氢离子、钠离子和硫酸根离子,可以根据检验产物中是否存在硫酸根离子,也可以将②的产物溶于水,有刺激性气味的气体二氧化硫产生.
解答 解:(1)根据题目的信息有极强的还原性.受热、遇水都会发生分解反应放出大量的热,甚至引起燃烧,所以保险粉要密封、阴凉处保存,故答案为:密封、阴凉处保存;
(2)①SO2中的硫+4价,而Na2S2O4中的硫+3价,所以硫的化合价降低,所以二氧化硫表现为氧化性,实验室用浓度较大的硫酸和亚硫酸盐反应,生成二氧化硫,盐酸易挥发,而稀硫酸溶液中水太多,大多数SO2生成了亚硫酸,不生成SO2气体,因为SO2易溶于水,1个体积的水溶解40个体积的SO2,硝酸有强氧化性,氧化二氧化硫,所以选择质量分数为70%的H2SO4,故答案为:氧化性;B;
②c(OH-)≥$\sqrt{\frac{Ksp}{c(Z{n}^{2+})}}$=$\sqrt{\frac{1{0}^{-17}}{1{0}^{-5}}}$=10-6mol∥L,所以pH≥8,故答案为:8;
③因为Na2S2O4易溶于水,但不溶于乙醇,所以可以用乙醇来洗涤沉淀,具体操作为:向漏斗中加少量无水乙醇至没过沉淀,滤干后重复操作2~3次,故答案为:向漏斗中加少量无水乙醇至没过沉淀,滤干后重复操作2~3次;
(3)根据反应硫的化合价+4价,而Na2S2O4中的硫+3价,化合价降价,根据电子得失守恒,HCOONa中的碳的化合价必然升高,由+2价变成+4价,所以缺项有+4价的碳,所以HCOONa和2Na2S2O4的系数相等,然后根据质量守恒分析得到:2HCOONa+4SO2+Na2CO3═2Na2S2O4+H2O+3CO2,故答案为:2、4、1、2、1、3CO2;
(4)反应①与反应②中都生成亚硫酸氢钠,而反应②中还产生硫酸氢钠,硫酸氢钠在水溶液中完全电离产生氢离子、钠离子和硫酸根离子,可以根据检验产物中是否存在硫酸根离子,具体操作为:取少许固体溶于水中,加入BaCl2溶液,有白色沉淀产生,则证明是②,故答案为:取少许固体溶于水中,加入BaCl2溶液,有白色沉淀产生,则证明是②.
点评 本题主要考查学生从题目中获取信息的能力以及根据获得的信息结合所学化学知识解决问题的能力,题目中用到的化学知识有根据电子得失守恒和质量守恒定律推断化学式、溶度积的相关计算、沉淀的洗涤和离子的检验等知识,综合性强,但难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Al3+>Mg2+>F- | B. | 热稳定性:HI>HBr>HCl>HF | ||
| C. | 酸性:H2SiO3<H3PO4<H2SO4<HClO4 | D. | 碱性:Al(OH)3>Mg(OH)2>NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用不活泼金属铜作电极电解饱和食盐水:2Cl-+2H2O═Cl2↑+H2↑+2OH- | |
| B. | HCO3-离子水解方程式:HCO3-+H2O═H3O++CO32- | |
| C. | 乙烯通入溴水中:C2H4+Br2═CH2BrCH2Br | |
| D. | 氯化铁溶液与碳酸氢钠溶液混合:Fe3++3HCO3-═Fe(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH | 加碱溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
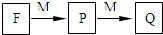 短周期主族元素A、B、C、D、E、F的原子序数依次增大.A和B形成4个原子核的分子,A和C形成3个原子核的分子,且两种分子均含有10个电子.D的阳离子的电子层结构与氖相同,且与A同主族.E的常见氧化物有两种,其中一种能使品红溶液褪色.
短周期主族元素A、B、C、D、E、F的原子序数依次增大.A和B形成4个原子核的分子,A和C形成3个原子核的分子,且两种分子均含有10个电子.D的阳离子的电子层结构与氖相同,且与A同主族.E的常见氧化物有两种,其中一种能使品红溶液褪色.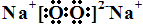 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
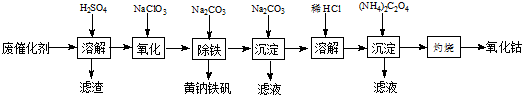

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com