
 .
. 分析 (1)稀有气体原子序数自上而下依次为2、10、18、36、54、86,82号元素与86号元素相差4,故二者同周期,82号元素处于第14列,即处于第六周期ⅣA族,为Pb元素,最高正化合价为+4,进而书写氧化物化学式;
(2)大多数的化合反应、所有燃烧反应、酸碱中和反应、金属与酸的反应等,属于放热反应,硫酸、氢氧化钠等溶解为放热过程;大多数的分解反应、以CO或碳或氢气为还原剂的反应、氢氧化钡与氯化铵的反应等,属于吸热反应,一些铵盐的溶解为吸热过程;
Ba(OH)2•8H2O与NH4Cl反应生成氯化钡、氨气与水;
(3)①铵盐是全部由非金属元素组成的离子化合物;
②只含共价键的化合物是共价化合物,不同非金属元素之间易形成极性共价键;
③同种非金属元素之间形成非极性共价键;
④活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性共价键;
⑤含有H原子的化合物,分子中一定不满足所有原子均满足8电子结构;
⑥Na2O由钠离子与氧离子构成,用Na原子、氧原子电子式表示其形成.
解答 解:(1)稀有气体原子序数自上而下依次为2、10、18、36、54、86,82号元素与86号元素相差4,故二者同周期,82号元素处于第14列,即处于第六周期ⅣA族,为Pb元素,最高正化合价为+4,最高价氧化物的化学式为PbO2,
故答案为:硫、ⅣA;PbO2;
(2)①木炭与水制备水煤气,属于吸热反应,②高锰酸钾的分解,属于吸热反应,③氢气与氯气混合见光爆炸,属于放热反应,④硫酸与烧碱反应,属于放热反应,⑤生石灰与水作用制熟石灰,属于放热反应,⑥Ba(OH)2•8H2O与NH4Cl,属于吸热反应,⑦硫酸溶解于水,属于放热过程,⑧硝酸铵溶解于水吸热过程,属于放热反应有③④⑤,反应⑥的化学方程式:Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O,
故答案为:③④⑤;Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;
(3)①铵盐是全部由非金属元素组成的离子化合物,符合条件的是氯化铵,故答案为:NH4Cl;
②只含共价键的化合物是共价化合物,不同非金属元素之间易形成极性共价键,只有极性键构成的共价化合物为CO2,故答案为:CO2;
③同种非金属元素之间形成非极性共价键,符合条件的是I2,故答案为:I2;
④活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性共价键,则符合条件的是Na2O2,故答案为:Na2O2;
⑤上述化合物中H2O2、NH4Cl不满足所有原子均满足8电子结构,故答案为:H2O2、NH4Cl;
⑥Na2O由钠离子与氧离子构成,用Na原子、氧原子电子式表示其形成为 ,
,
故答案为: .
.
点评 本题考查位置结构性质关系、吸热反应与放热反应、化学键等,属于拼合型题目,需要学生熟练掌握基础知识,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 电子有得失 | B. | 共用电子对有偏移 | ||
| C. | 电子既有得失又有偏移 | D. | 金属元素的存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2CO3>H2SiO3>H3PO4 | B. | 碱性:CsOH>Ba(OH)2>Ca(OH)2 | ||
| C. | 热稳定性:H2O>HF>NH3>HCl | D. | 氧化性:Ag+<Cu2+<H+<Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
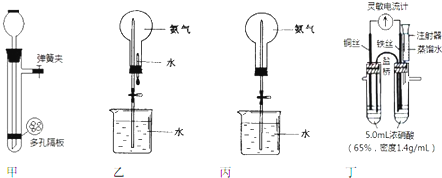
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO 0.001 mol•L-1 | B. | H2O 0.002 mol•L-1 | ||
| C. | NH3 0.002 mol•L-1 | D. | O2 0.0025 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 非金属元素H、C、N、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛,完成下列各题.
非金属元素H、C、N、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛,完成下列各题.| 危险性 |  |
| 储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 | NaOH、NaHSO3溶液吸收 |
| 包装 | 钢瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

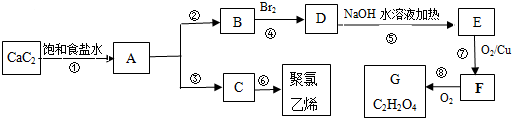
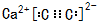 ,A的结构式H-C≡C-H,B分子中碳原子的杂化方式是sp2
,A的结构式H-C≡C-H,B分子中碳原子的杂化方式是sp2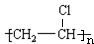 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com