
| A. | NH4Br的电子式: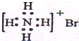 | |
| B. | S2-的结构示意图: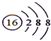 | |
| C. | 乙酸的分子式:CH3COOH | |
| D. | 原子核内有18个中子的氯原子:37Cl |
分析 A.铵根离子和溴离子都需要标出所带电荷和原子的最外层电子,溴离子为阴离子,电子式中需要标出最外层的8个电子;
B.硫离子的核外电子总数18,最外层为8个电子;
C.分子式中不需要标出官能团结构,图为该物质的结构简式;
D.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数.
解答 解:A.溴化铵是离子化合物,由铵根离子与溴离子构成,电子式为: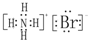 ,故A错误;
,故A错误;
B.硫离子的核电荷数为16,核外电子总数为18,最外层为8个电子,硫离子的结构示意图为: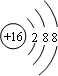 ,故B正确;
,故B正确;
C.乙酸分子中含2个C、4个H,2个O,且含羧基,结构简式为CH3COOH,分子式为C2H4O2,故C错误;
D.原子核内有l8个中子的氯原子的质量数=质子数+中子数=17+18=35,该原子可以表示为:$\underset{\stackrel{35}{\;}}{17}\underset{\stackrel{\;}{Cl}}{\;}$,故D错误;
故选B.
点评 本题考查常用化学用语书写,题目难度不大,注意掌握电子式、离子结构示意图与原子结构示意图、分子式、元素符号等常用化学用语的书写原则.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去AlCl3溶液中的FeCl3杂质的方法:先加入足量浓氨水,过滤,再加入过量盐酸,得到纯净AlCl3溶液 | |
| B. | 可以用金属钠和MgCl2溶液反应置换金属Mg;可以通过化合反应制备Fe(OH)3 | |
| C. | 对某溶液进行焰色反应,火焰呈黄色,则证明该溶液中含有钠盐,可能有钾盐 | |
| D. | 配制氯化铁溶液时,将氯化铁固体溶解在较浓的盐酸中再加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
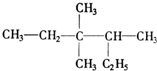 3,3,4-三甲基己烷;
3,3,4-三甲基己烷;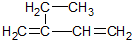 2-乙基-1,3-丁二烯.
2-乙基-1,3-丁二烯.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 验证某有机物属于烃,完成的实验只要证明它完全燃烧后的产物只有H2O和CO2 | |
| B. | 煤干馏得到的煤焦油可以分离出苯,苯是无色无味的液态烃 | |
| C. | 黄酒中存在的某些微生物可以使部分乙醇氧化,转化为乙酸,酒就有了酸味 | |
| D. | 乙烯使酸性高锰酸钾溶液,溴的四氯化碳溶液褪色,由于乙烯发生了加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 溶液酸性越强,R 的降解速率越小 | |
| B. | R的起始浓度越小,降解速率越大 | |
| C. | 在0~50 min之间,pH=2和PH=7时R的降解百分率相等 | |
| D. | 在20~25 min之间,pH=10 时R的平均降解速率为0.04 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A. | 容器①、②中反应的平衡常数相等 | |
| B. | 平衡时,两个容器中NH3的体积分数均为25% | |
| C. | 容器②中达平衡时放出的热量Q=23.15 kJ | |
| D. | 若容器①体积为0.5L,则平衡时放出的热量<23.15kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 L CO和CO2的混合气体中所含的碳原子数一定是NA | |
| B. | 标准状况下,22.4 L氖气含有原子数为NA | |
| C. | 物质的量浓度为2 mol/L的BaCl2溶液中,含有Cl-个数为4NA | |
| D. | 标准状况下,11.2 L H2O含有0.5NA分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com