
【题目】标况下,一容积不变的密闭容器里充满硫化氢和氧气的混合气体,点燃恰好完全反应后,恢复至原状态,压强变为原来的![]() ,计算原混合气体的硫化氢和氧气的体积比________。
,计算原混合气体的硫化氢和氧气的体积比________。
【答案】4∶5
【解析】
硫化氢燃烧可以发生反应:①2H2S+O2![]() 2S+2H2O,②2H2S+3O2
2S+2H2O,②2H2S+3O2![]() 2SO2+2H2O,反应前后都在标况下,恢复至原状态,若只发生①,反应后压强为0;若只发生反应②,反应后压强变为原来的
2SO2+2H2O,反应前后都在标况下,恢复至原状态,若只发生①,反应后压强为0;若只发生反应②,反应后压强变为原来的![]() ,根据方程式对应关系可以求得答案。
,根据方程式对应关系可以求得答案。
硫化氢燃烧可以发生反应:①2H2S+O2![]() 2S+2H2O,②2H2S+3O2
2S+2H2O,②2H2S+3O2![]() 2SO2+2H2O,反应前后都在标况下,恢复至原状态,若只发生①,反应后压强为0;若只发生反应②,反应后压强变为原来的
2SO2+2H2O,反应前后都在标况下,恢复至原状态,若只发生①,反应后压强为0;若只发生反应②,反应后压强变为原来的![]() 。由题目信息得压强变为原来的
。由题目信息得压强变为原来的![]() ,则反应①、②都发生。又根据相同条件下压强之比等于气体物质的量之比,假设反应后气体物质的量为1mol,即反应后二氧化硫的物质的量为1mol,则反应前混合气体总物质的量为3 mol,则根据反应:
,则反应①、②都发生。又根据相同条件下压强之比等于气体物质的量之比,假设反应后气体物质的量为1mol,即反应后二氧化硫的物质的量为1mol,则反应前混合气体总物质的量为3 mol,则根据反应:
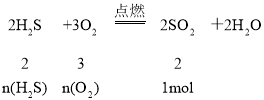
n(H2S)=1mol,n(O2)=1.5mol,消耗的H2S和O2分别为1mol和1.5mol,故硫化氢燃烧生成硫与水的反应中,n(H2S)+n(O2)=3mol-1mol-1.5mol=0.5 mol。由反应:2H2S+O2![]() 2S↓+2H2O,可知n(H2S)=0.5 mol×
2S↓+2H2O,可知n(H2S)=0.5 mol×![]() =
=![]() mol,n(O2)=0.5 mol×
mol,n(O2)=0.5 mol×![]() =
=![]() mol。原混合气体的硫化氢和氧气的体积比等于其物质的量之比,为(1 mol+
mol。原混合气体的硫化氢和氧气的体积比等于其物质的量之比,为(1 mol+![]() mol)∶(1.5 mol+
mol)∶(1.5 mol+![]() mol)=4∶5。
mol)=4∶5。


科目:高中化学 来源: 题型:
【题目】丙烯酰胺是一种重要的有机合成的中间体。它的球棍模型如图所示:(图中“棍”代表单键或双键或三键,不同颜色球表示不同原子:C、H、O、N)

(1)丙烯酰胺的分子式为___,结构简式为___。
(2)有关丙烯酰胺的说法正确的是___。
A.丙烯酰胺分子内所有原子不可能在同一平面内
B.丙烯酰胺属于烃的含氧衍生物
C.丙烯酰胺能够使酸性高锰酸钾溶液褪色
D.丙烯酰胺能够使溴的四氯化碳溶液褪色
(3)工业上生产丙烯酰胺可以用下面的反应(反应均在一定条件下进行):
CH![]() CH
CH![]() CH2=CHCN
CH2=CHCN![]() 丙烯酰胺
丙烯酰胺
假设反应Ⅰ和反应Ⅱ都是原子利用率100%的反应,反应Ⅰ所需另一反应物的分子式为___,反应Ⅱ的方程式为___。
(4)聚丙烯酰胺(PAM)是一种合成有机高分子絮凝剂,写出由丙烯酰胺合成聚丙烯酰胺的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 室温下,向苯酚钠溶液中通足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
B | 加热乙醇与浓硫酸的混合溶液,将产生的气体通入少量酸性KMnO4溶液,溶液紫红色褪去 | 有乙烯生成 |
C | 向5 mL 0.1 mol·L1 KI溶液中加入1 mL 0.1 mol·L1 FeCl3溶液,充分反应后,萃取分液,向水层中滴加KSCN溶液,溶液呈血红色 | I-与Fe3+的反应有一定限度 |
D | 向NaHCO3溶液中滴加紫色石蕊试液,溶液变蓝 | Kw<Ka1(H2CO3)×Ka2(H2CO3) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双缩脲反应可以用于测定蛋白质的含量。双缩脲反应的原理可表示如下:

双缩脲 紫红色配离子
(1)Cu2+的基态核外电子排布式为_______。
(2)与H2O互为等电子体的一种阳离子为_______(填化学式)。
(3)双缩脲分子中氮原子轨道的杂化类型是_______;1 mol双缩脲分子中含有σ键的数目为_______。
(4)该紫红色配离子中的配位原子为_______。
(5)Cu3Au的晶胞如下图所示,Cu3Au晶体中每个铜原子周围距离最近的铜原子数目为_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴是一种重要的化工材料,广泛应用于有机合成。一种以铜钴矿(主要成分为Co2CuS4,一定量CuFeS2)为原料,生产草酸钴晶体(CoC2O4·2H2O)的工艺流程:
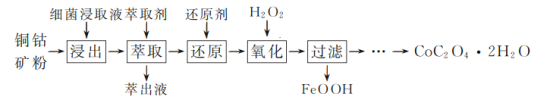
已知:①“浸出”液含有的离子主要有H+、Fe3+、Cu2+、Co3+、![]() ;
;
②pH增大,Fe2+被氧化的速率加快,同时生成的Fe3+水解形成更多的胶体;
③草酸钴晶体难溶于水;25℃时,Ksp[Co(OH)2]=1.6×10-15。
回答下列问题:
(1)生产时为提高铜钴矿粉浸出率,常采取的措施有________(填字母)。
a.适当延长浸出时间b.高温浸出c.分批加入细菌浸取液并搅拌
(2)“萃取”步骤中萃取除去的主要金属阳离子是________。
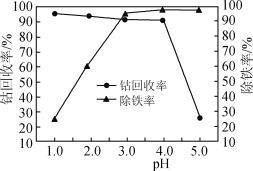
(3)“氧化”过程中,控制70℃、pH=4条件下进行,pH对除铁率和钴回收率的影响如图所示。
①用电子式表示H2O2的形成过程________。
②“氧化”过程的离子方程式为________。
③pH为4~5时,钴的回收率降低的原因是________。
(4)“过滤”后的滤液中加入(NH4)2C2O4溶液反应得到草酸钴晶体,过滤得到的草酸钴晶体需要用蒸馏水洗涤,检验晶体是否洗涤干净的方法是_______________。
(5)300℃时,在空气中煅烧CoC2O4·2H2O可制得Co3O4,该反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤。图示装置和原理不合理的是
A.制取氨气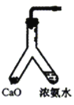 B.制取NaHCO3
B.制取NaHCO3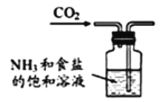
C.分离NaHCO3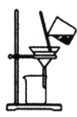 D.干燥NaHCO3
D.干燥NaHCO3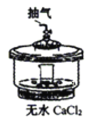
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H 1=-90.7 kJ·mol-1 K1
CH3OH(g) △H 1=-90.7 kJ·mol-1 K1
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1 K2
CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1 K2
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H 3=-41.2kJ·mol-1 K3
CO2(g)+H2(g) △H 3=-41.2kJ·mol-1 K3
回答下列问题:
(1)则反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)的△H=____kJ·mol-1;该反应的平衡常数K=____(用K1、K2、K3表示)
CH3OCH3(g)+CO2(g)的△H=____kJ·mol-1;该反应的平衡常数K=____(用K1、K2、K3表示)
(2)下列措施中,能提高CH3OCH3产率的有____。
A.使用过量的CO B.升高温度 C.增大压强
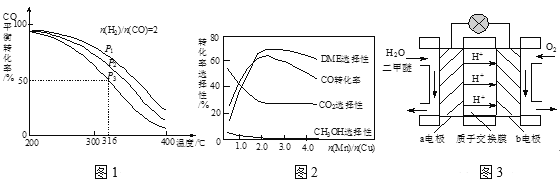
(3)将合成气以n(H2)/n(CO)=2通入1 L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)![]() CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图1所示,下列说法正确的是____。
CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图1所示,下列说法正确的是____。
A.△H <0
B.P1>P2>P3:
C.若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50%
(4)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚。观察图2回答问题。催化剂中n(Mn)/n(Cu)约为____时最有利于二甲醚的合成。
(5)图3为绿色电源“二甲醚燃料电池”的工作原理示意图,a电极的电极反应式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.![]() 、
、![]() 、
、![]() 三种核素最多可以组成2种水分子
三种核素最多可以组成2种水分子
B.核内中子数为N的R2+,质量数为A,则该粒子的核外电子数为:A-N-2
C.CH3OH和CH3-O-CH3分子组成相差一个CH2,所以互为同系物
D.按系统命名法,化合物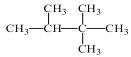 的名称为2,3,3-三甲基丁烷
的名称为2,3,3-三甲基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在800℃时,2L密闭容器内发生反应:2NO(g)+O2(g)2NO2(g),反应体系中,一氧化氮的物质的量随时间的变化如表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)如图表示NO2的物质的量浓度变化的曲线是________。
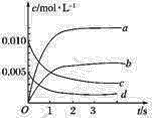
(2)用O2表示从0~2 s内该反应的平均速率v=__________。
(3)能说明该反应已达到平衡状态的是________。
A.v(NO2)=2v(O2)
B.容器内压强保持不变
C.容器内气体质量不变
D.容器内密度保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com