
下列说法不正确的是 ( )
A.(NH4)2SO4和CuSO4溶液都能使蛋白质沉淀析出
B. 苯酚与甲醛在酸性条件下生成酚醛树脂的结构简式为 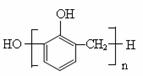
C.醋酸和硬脂酸互为同系物,C6H14和C9H20也一定互为同系物
D.叶酸的结构为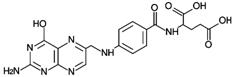 ,它可以发生酯化、水解、加成等反应
,它可以发生酯化、水解、加成等反应
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
某研究性学习小组为了测定某品牌合金中铝的含量,现设计了如下实验:
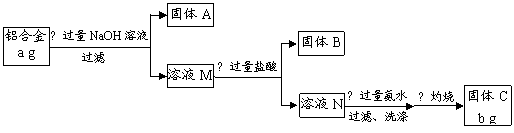 |
已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
请回答下列问题:
(1)固体A的成分是 ▲ ;
(2)生成固体B的离子方程式为 ▲ ;
步骤③中生成沉淀的离子方程式为 ▲ ;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为 ▲
;
(4)该样品中铝的质量分数是 ▲ ;(用a、b表示)
(5)下列因操作不当,会使测定结果偏大的是 ▲ ;
A.第①步中加入NaOH溶液不足 B.第②步中加入盐酸不足时
C.第③步中沉淀未用蒸馏水洗涤 D.第④步对沉淀灼烧不充分
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2是最重要温室气体,如何降低大气中CO2的含量及有效地开发利用CO2具有重大意义。
 (1)科学家用H2和CO2生产甲醇燃料。为探究该反应原理,进行如下实验:某温度下,在容积为2 L的密闭容器中充入1 mol CO2和3.25 mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。
(1)科学家用H2和CO2生产甲醇燃料。为探究该反应原理,进行如下实验:某温度下,在容积为2 L的密闭容器中充入1 mol CO2和3.25 mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。
①从反应开始到3 min时,氢气的平均反应速率v(H2)=________。
②下列措施中一定能使CO2的转化率增 大的是_______。
大的是_______。
A.在原容器中再充入1 mol H2
B.在原容器中再充入1 mol CO2
C.缩小容器的容积
D.使用更有效的催化剂
E.在原容器中充入1 mol He
F.将水蒸气从体系中分离出
(2)科学家还利用氢气在一定条件下与二氧化碳反应生成乙醇燃料,其热化学反应方程式为:
2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,在一定压强下,测得该反应的实验数据如表所示。
CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,在一定压强下,测得该反应的实验数据如表所示。
请根据表中数据回答下列问题。
|
n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
①上述反应的a________0(填“大于”或“小于”)。
②恒温下,向反应体系中加入固体催化剂,则该反应的反应热a值________(填“增大”、“减小”或“不变”)。
③增大的值,则生成乙醇的物质的量________(填“增大”、“减小”、“不变”或“不能
确定”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于反应K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O的有关叙述中,正确的是
A. KCl中含有35Cl
B. 生成物Cl2的相对分子质量为73.3
C.该反应转移的电子数为6e-
D.氧化剂和还原剂的物质的量之比为1:6
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.离子晶体的晶格能越大,离子键越强
B.阳离子的半径越大则可同时吸引的阴离子越多
C.通常阴、阳离子的半径越小、电荷越大,该阴阳离子组成的离子化合物的晶格能越大
D.拆开1mol离子键所需的能量叫该离子晶体的晶格能
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表,相关说法正确的是
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
A.离子半径大小:r(M3+) >r(T2-) B.其中R的金属性最强
C.煤和石油中存在X元素 D.L、X形成的简单离子核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列叙述正确的是
A.lmol FeI2与足量氯气反应时转移的电子数为2NA
B.乙烯和丙烯组成的42 g混合气体中氢原子的个数为6 NA
C.1 mol Na2O2固体中含离子总数为4NA
D.2 L0.5 mol • L-1硫酸钾溶液中阴离子所带电荷数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
右图表示水中c(H+)和c(OH-)的关系,下列判断错误的是
A.图中T1<T2
B.两条曲线上任意点均有c(H+)×c(OH-)=Kw
C.M区域内任意点均有c(H+)<c(OH-)
D.XZ线上任意点均有pH=7

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com