
 阿司匹林可由水杨酸与乙酸酐作用制得.其制备原理如下:
阿司匹林可由水杨酸与乙酸酐作用制得.其制备原理如下: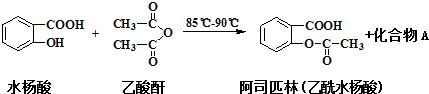

 ;
;分析 (1)主反应中水杨酸和乙酸酐发生取代反应生成阿司匹林,同时生成乙酸(CH3COOH);
(2)发生反应时温度控制在85~90℃,需要测量温度的仪器;测量的温度是水浴温度;
冷凝管起冷凝回流作用;用冷凝管冷却蒸气时,冷凝管中水流方向为逆流;
(3)乙酰水杨酸和碳酸氢钠反应生成二氧化碳和水,水杨酸发生缩聚反应生成聚水杨酸,聚水杨酸难溶于水;
(4)滤液中主要成分是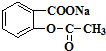 ,
,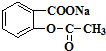 和稀盐酸反应生成阿司匹林;
和稀盐酸反应生成阿司匹林;
(5)阿司匹林和双氧水的区别是水杨酸含有酚羟基、阿司匹林含有酯基,可以用氯化铁溶液检验酚羟基;
如果阿司匹林中含有水杨酸,需要除去水杨酸得到较纯净的阿司匹林.
解答 解:(1)主反应中水杨酸和乙酸酐发生取代反应生成阿司匹林,根据取代反应特点知同时生成乙酸(CH3COOH),故答案为:乙酸(CH3COOH);
(2)发生反应时温度控制在85~90℃,需要测量温度的仪器,为温度计;测量的温度是水浴温度,所以温度计的水银球应该浸在水浴中,且不能触及容器底部;
冷凝管起冷凝回流作用;用冷凝管冷却蒸气时,冷凝管中水流为逆流,所以b进水口;
故答案为:温度计;温度计的水银球浸在水浴中,但不触及容器底部;冷凝回流;b;
(3)乙酰水杨酸和碳酸氢钠反应生成二氧化碳和水,水杨酸发生缩聚反应生成聚水杨酸,聚水杨酸难溶于水,所以得到的固体是聚水杨酸,
故答案为:聚水杨酸;
(4)滤液中主要成分是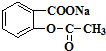 ,
,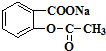 和稀盐酸反应生成阿司匹林,反应方程式为
和稀盐酸反应生成阿司匹林,反应方程式为 ,故答案为:
,故答案为: ;
;
(5)阿司匹林和双氧水的区别是水杨酸含有酚羟基、阿司匹林含有酯基,可以用氯化铁溶液检验酚羟基,检验方法为:取少量步骤5获得的晶体于试管中,加入适量的水溶解,再加入1~2滴三氯化铁溶液,若溶液变紫色,则有水杨酸,若溶液没有变紫色,则没有水杨酸;
如果阿司匹林中含有水杨酸,需要除去水杨酸得到较纯净的阿司匹林,应该采用重结晶方法,
故答案为:取少量步骤5获得的晶体于试管中,加入适量的水溶解,再加入1~2滴三氯化铁溶液,若溶液变紫色,则有水杨酸,若溶液没有变紫色,则没有水杨酸;重结晶.
点评 本题考查物质制备实验方案设计,为高频考点,明确实验原理是解本题关键,知道每个实验步骤目的及基本操作方法,易错点是冷凝管中水流方向判断,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 正丁醚是惰性溶剂,可用作有机合成反应溶剂.某实验小组利用如下装置(夹持和加热装置均省略)合成正丁醚.发生的反应为:
正丁醚是惰性溶剂,可用作有机合成反应溶剂.某实验小组利用如下装置(夹持和加热装置均省略)合成正丁醚.发生的反应为:| 化合物 名称 | 密度(g/mL ) | 熔 点(℃) | 沸 点(℃) | 水中溶解性 |
| 正丁醇 | 0.810 | -89.8 | 118.0 | 微溶 |
| 正丁醚 | 0.7689 | -95.3 | 142 | 不溶于水 |
| 备注:正丁醚微溶于饱和氯化钙溶液. | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是理想,更是一种值得期待的新的生活方式,请运用化学反应原理的相关知识研究碳及其化合物的性质.
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是理想,更是一种值得期待的新的生活方式,请运用化学反应原理的相关知识研究碳及其化合物的性质.| 温 度 | 250℃ | 300℃ | 350℃ |
| Κ | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 组分 | 物质的量/mol |
| HCOOCH3 | 1.00 |
| H2O | 1.99 |
| HCOOH | 0.01 |
| CH3OH | 0.52 |

| A. | 温度升髙,该反应的平衡常数减小 | |
| B. | 0〜10min,HCOOCH3的平均反应速率v=0.003mol•L-1min-1 | |
| C. | HCOOCH3水解平均反应速率先是增大,后减小,最后保持不变 | |
| D. | 该条件下达到平衡状态,反应物转化率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
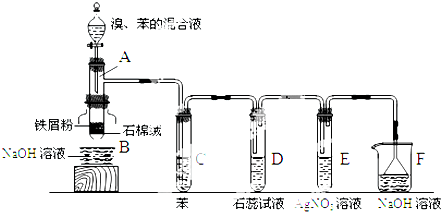
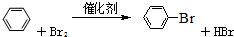 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
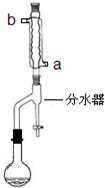 在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.
在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种溶液中的c(Na+)相等 | |
| B. | 分别加水稀释到100 mL时,两种溶液的pH依然相等 | |
| C. | 两溶液中由水电离出的c(OH-)之比为10-9/10-5 | |
| D. | 分别与同浓度的盐酸反应,pH=7时消耗的盐酸体积相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200ml 2mol/L Mg Cl2溶液 | B. | 1000 ml 2.5 mol/LNaCl | ||
| C. | 300 ml 5 mol/L K Cl 溶液 | D. | 250 ml 1 mol/L AlCl3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com