
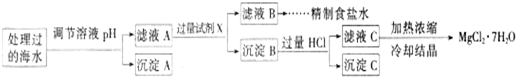
£Ø2012?ŹÆ¼Ņ×ÆÄ£Äā£©æĘѧ¼ŅŅ»Ö±ÖĀĮ¦ÓŚ”°ČĖ¹¤¹ĢµŖ”±µÄ·½·ØŃŠ¾æ£®
£Ø1£©ŗĻ³É°±µÄŌĄķĪŖ£ŗN
2£Øg£©+3H
2£Øg£©?2NH
3£Øg£©”÷H=-92.4kJ/mol£¬øĆ·“Ó¦µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£®
¢ŁŌŚ·“Ó¦ĢåĻµÖŠ¼ÓČė“߻ƼĮ£¬·“Ó¦ĖŁĀŹŌö“ó£¬E
2µÄ±ä»ÆŹĒ
¼õŠ”
¼õŠ”
£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£®
¢Ś½«0.3mol N
2ŗĶ0.5mol H
2³äČėĢå»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗā£¬²āµĆČŻĘ÷ÄŚĘųĢåŃ¹Ēæ±äĪŖŌĄ“µÄ
£¬“ĖŹ±H
2µÄ×Ŗ»ÆĀŹĪŖ
30%
30%
£»ÓūĢįøßøĆČŻĘ÷ÖŠH
2µÄ×Ŗ»ÆĀŹ£¬ĻĀĮŠ“ėŹ©æÉŠŠµÄŹĒ
AD
AD
£ØĢīŃ”Ļī×ÖÄø£©£®
A£®ĻņČŻĘ÷ÖŠ°“Ō±ČĄżŌŁ³äČėŌĮĻĘų B£®ĻņČŻĘ÷ÖŠŌŁ³äČėŅ»¶ØĮæH
2C£®øı䷓ӦµÄ“߻ƼĮ D£®Ņŗ»ÆÉś³ÉĪļ·ÖĄė³ö°±
£Ø2£©øł¾Ż×īŠĀ”°ČĖ¹¤¹ĢµŖ”±µÄŃŠ¾æ±ØµĄ£¬ŌŚ³£ĪĀ”¢³£Ń¹”¢¹āÕÕĢõ¼žĻĀ£¬N
2ŌŚ“߻ƼĮ£Ø²ōÓŠÉŁĮæFe
2O
3ŗĶTiO
2£©±ķĆęÓėĖ®·¢Éś·“Ó¦£ŗ
2N
2£Øg£©+6H
2O£Ø1£©?4NH
3£Øg£©+3O
2£Øg£©”÷H=+1530kJ/mol
ÓÖÖŖ£ŗH
2O£Ø1£©=H
2O£Øg£©”÷H=+44.0kJ/mol
Ōņ2N
2£Øg£©+6H
2O£Øg£©?4NH
3£Øg£©+3O
2£Øg£©”÷H=
+1266
+1266
kJ/mol£¬øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ĪŖK=
| C4(NH3)C3(O2) |
| C2(N2)C6(H2O) |
£¬
| C4(NH3)C3(O2) |
| C2(N2)C6(H2O) |
£¬
£¬æŲÖĘĘäĖūĢõ¼ž²»±ä£¬Ōö“óŃ¹Ē棬KÖµ
²»±ä
²»±ä
£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£®

 £Ø2012?ŹÆ¼Ņ×ÆÄ£Äā£©æĘѧ¼ŅŅ»Ö±ÖĀĮ¦ÓŚ”°ČĖ¹¤¹ĢµŖ”±µÄ·½·ØŃŠ¾æ£®
£Ø2012?ŹÆ¼Ņ×ÆÄ£Äā£©æĘѧ¼ŅŅ»Ö±ÖĀĮ¦ÓŚ”°ČĖ¹¤¹ĢµŖ”±µÄ·½·ØŃŠ¾æ£®

 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
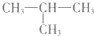 £Ø2012?ŹÆ¼Ņ×ÆŅ»Ä££©2-¼×»ł±ūĶé£ØČēĶ¼£©µÄ¶žĀČ“śĪļ¹²ÓŠ£Ø²»æ¼ĀĒĮ¢ĢåŅģ¹¹£©£Ø””””£©
£Ø2012?ŹÆ¼Ņ×ÆŅ»Ä££©2-¼×»ł±ūĶé£ØČēĶ¼£©µÄ¶žĀČ“śĪļ¹²ÓŠ£Ø²»æ¼ĀĒĮ¢ĢåŅģ¹¹£©£Ø””””£©