
【题目】工业上设计用CO2来生产燃料甲醇,既减少二氧化碳气体,又得到宝贵的能源物质.为了探究反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1molCO2和3molH2 , 某温度下发生反应:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=﹣49.0KJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示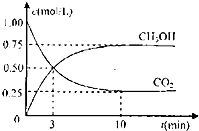
(1)该反应该温度下,化学平衡常数的值为
(2)下列说法中能作为反应达到平衡状态标志的是(填字母).
A.容器内压强不再发生变化
B.平均相对分子质量不再变化
C.c(CO2)和c(H2)之比等于1:3
D.相同时间内每断裂3molH﹣H键,同时断裂3molO﹣H键
(3)下列措施中能使 ![]() 减小的是
减小的是
A.再充入1molCO2和3molH2
B.将H2O(g)从体系中分离
C.充入He(g),使体系压强增大
D.升高温度.
【答案】
(1)5.33
(2)A,B,D
(3)D
【解析】解:(1.)图象中得到平衡状态二氧化碳浓度为0.25mol/L,甲醇浓度为0.75mol/L,利用化学平衡三行计算方法得到,
CO2(g)+3H2(g)CH3OH(g)+H2O(g),
开始(mol/L): 1 3 0 0
变化(mol/L): 0.75 2.25 0.75 0.75
平衡(mol/L): 0.25 0.75 0.75 0.75
平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,则K= ![]() =
= ![]() =5.33,
=5.33,
所以答案是:5.33;
(2.)CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=﹣49.0KJ/mol,反应是气体体积减小的放热反应,
A.反应前后气体物质的量变化,当容器内压强不再发生变化,说明反应达到平衡状态,故A正确;
B.反应前后气体物质的量变化,气体质量不变,若平均相对分子质量不再变化,说明反应达到平衡状态,故B正确;
C.c(CO2)和c(H2)之比等于1:3是反应之比,不能说明正逆反应速率相同,故C错误;
D.生成物中H﹣O键不是一种物质中的化学键,甲醇和水分子中H﹣O键一定是1:2,依据化学方程式可知相同时间内每断裂3molH﹣H键,同时断裂3molO﹣H键,能说明正逆反应速率相同,故D正确;
故选ABD.
(3.)要使 ![]() 减小,应使平衡向逆反应方向移动,
减小,应使平衡向逆反应方向移动,
A.再充入1mol CO2和3mol H2 , 增大反应物浓度,平衡向正反应方向移动,则比值增大,故A错误;
B.将H2O(g)从体系中分离,平衡向正反应方向移动,比值增大,故B错误;
C.充入He(g),使体系压强增大,但对反应物质来说,浓度没有变化,平衡不移动,比值不变,故C错误;
D.因正反应放热,升高温度平衡向逆反应方向移动,则比值减小,故D正确;
所以答案是:D;
【考点精析】利用化学平衡状态本质及特征和化学平衡状态的判断对题目进行判断即可得到答案,需要熟知化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等.


科目:高中化学 来源: 题型:
【题目】下列描述前者属于化学变化,后者属于物理变化的是( )
A. 汽油挥发 酒精燃烧 B. 食物腐烂 水蒸发
C. 铁铸成锅 蜡烛燃烧 D. 滴水成冰 水加热变成水蒸气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.在电解池中,物质在阴极发生氧化反应
B.在电解池中,与电源正极相连的电极是阴极
C.在原电池中,物质在负极发生氧化反应
D.在原电池中,电子由正极流向负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种香料,存在于金橘中,可用如下路线合成: 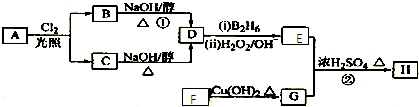
已知:R﹣CH=CH2 ![]() R﹣CH2CH2OH(B2H6为乙硼烷)
R﹣CH2CH2OH(B2H6为乙硼烷)
回答下列问题:
(1)11.2L(标准状况)的烃A在氧气中充分燃烧可以产生88g CO2和45g H2O.A的分子式是
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为
(3)在催化剂存在下1mol F与2mol H2反应,生成3﹣苯基﹣1﹣丙醇.F的结构简式是
(4)反应①的反应类型是;
(5)反应②的化学方程式为
(6)写出所有与G具有相同官能团的G的芳香类同分异构体的结构简式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上冶炼冰铜(mCu2OnFeS)可得到粗铜,冰铜与酸反应可以生成硫化氢(见图1).完成下列填空: 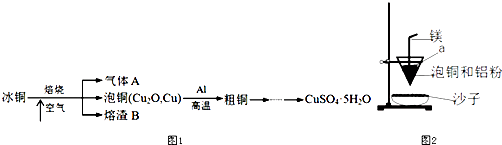
(1)气体A中的大气污染物可选用下列试剂中的(填序号)吸收.
a.浓H2SO4 b.浓HNO3 c.NaOH溶液 d.氨水
(2)实验室可用如图2的装置完成泡铜冶炼粗铜的反应.
①泡铜冶炼粗铜的化学方程式是;
②装置中镁带的作用是;
③泡铜和铝粉混合物表面覆盖少量白色固体a,a是;
(3)将H2S和O2在密闭容器中点燃,充分反应后恢复到原来的温度和压强(120℃、101kPa),气体体积减少30%,求原混合其气体中H2S的体积分数 . (不考虑H2S的自身分解)已知:氧气不足时:2H2S+O2 ![]() 2S+2H2O 氧气足量时:2H2S+3O2═2SO2+2H2O;
2S+2H2O 氧气足量时:2H2S+3O2═2SO2+2H2O;
(4)已知:SiCl4(s)+H2(g)═SiHCl3(s)+HCl(g)△H1=47kJ/mol
SiHCl3(s)+H2(g)═Si(s)+3HCl(g)△H2=189kJ/mol
则由SiCl4制备硅的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠是一种高效氧化剂漂白剂,主要用于 棉纺、亚麻、纸浆等漂白亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2﹣、Cl﹣等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl﹣没有画出).则下列分析不正确的是( ) 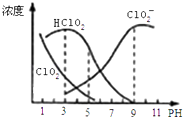
A.亚氯酸钠在碱性条件下较稳定
B.25℃时,HClO2的电离平衡常数的数值Ka=10﹣6
C.使用该漂白剂的最佳pH为3
D.25℃时,同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)+2c(H+)=c(ClO2﹣)+2c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在NaCl、MgCl2、MgSO4的混合溶液中,c(Na+)=0.10mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.20mol/L,则c(SO42-)为
A. 0.10mol/L B. 0.15mol/L C. 0.20mol/L D. 0.25mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中的△H可表示燃烧热的是( )
A.H2(g)+Cl2(g)═2HCl(g)△H=﹣184.8KJ/mol
B.C2H4(g)+O2(g)═2CO2(g)+2H2O(l)△H=﹣1411.0KJ/mol
C.CH4(g)+ ![]() O2(g)═CO(g)+2H2O(l)△H=﹣6071.3KJ/mol
O2(g)═CO(g)+2H2O(l)△H=﹣6071.3KJ/mol
D.H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8KJ/mol
O2(g)═H2O(g)△H=﹣241.8KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家冶炼出了纯度高达99.9999%的铁,你估计它不会具有的性质是
A.在潮湿的空气中放置不易生锈B.硬度比生铁大
C.与2mol/L盐酸的反应生成氢气D.在冷的浓H2SO4溶液中可钝化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com