
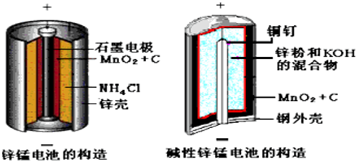
分析 (1)酸性锌锰干电池的负极为锌;
(2)正极上二氧化锰得电子发生还原反应生成MnOOH;
(3)持电流强度为0.6A,电池工作10分钟,则电量为0.6A×600s=360C,转移电子的物质的量为$\frac{360C}{96500C/mol}$=0.00373mol,以此计算消耗锌的质量.
解答 解:(1)酸性锌锰干电池的负极为锌,负极反应为Zn-2e-=Zn2+,
故答案为:Zn-2e-=Zn2+;
(2)在碱性锌锰原电池中,Zn易失电子作负极、二氧化锰作正极,正极上二氧化锰得电子发生还原反应,电极反应式为MnO2+e-+H2O=MnOOH+OH-,
故答案为:MnO2+e-+H2O=MnOOH+OH-;
(3)持电流强度为0.6A,电池工作10分钟,则电量为0.6A×600s=360C,转移电子的物质的量为$\frac{360C}{96500C/mol}$=0.00373mol则消耗Zn的质量为0.00373mol×$\frac{1}{2}$×65g/mol=0.12g,
故答案为:0.12.
点评 本题考查普通干电池的工作原理,有利于培养学生良好的科学素养,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 略小于20% | B. | 略大于20% | C. | 20% | D. | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有乙烷 | B. | 一定是甲烷和乙烯 | ||
| C. | 一定有甲烷 | D. | 一定有乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 的正确命名为( )
的正确命名为( )| A. | 2,3,3-三甲基戊烷 | B. | 3,3,4-三甲基已烷 | ||
| C. | 3,3-二甲基-4-乙基戊烷 | D. | 2-乙基-3,3-二甲基-4-乙基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
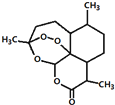
| A. | 用沸点只有35℃的乙醚作为溶剂来提取青蒿素的方法化学上叫萃取 | |
| B. | 能够发生水解反应 | |
| C. | 分子式为C15H23O5 | |
| D. | 青蒿素能够治疗疟疾可能与结构中存在过氧键或酯基等基团有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
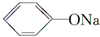 +CH3I→
+CH3I→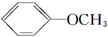 +NaI
+NaI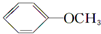 +HI→
+HI→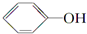 +CH3l
+CH3l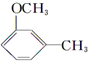 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$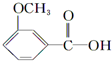
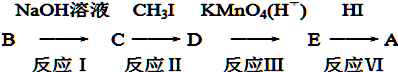
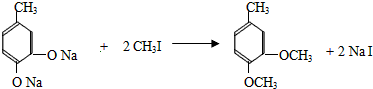 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com