
某研究性学习小组用FeCl3溶液做“腐蚀液”,制作印刷电路板,其反应原理是:2FeCl3+Cu=2FeCl2+CuCl2。
【实验探究】
(1)通过《化学1》的学习,知道了有离子参加的化学反应为离子反应。离子反应可用离子方程式表示。请写出2FeCl3+Cu=2FeCl2+CuCl2反应的离子方程式为: 。
(2)若要溶解电路板上3.2g的铜,则至少需要FeCl3物质的量为 mol。
(3)使用后失效的“腐蚀液”为废液,验证废液中是否存在Fe3+的试剂是 ,加入该试剂后,若出现 现象,说明废液中还存在Fe3+。
(4)废液中的CuCl2可通过加入足量的 ,反应后转化成铜且能使所得溶液中含有单一溶质。
(5)回收Cu后的废液,通入足量的Cl2,可以重新获得FeCl3溶液,其反应的化学方程式为 。
【实验结论】
利用FeCl3溶液做印刷电路板的“腐蚀液”,不仅废液中的铜可以得到回收,经过处理后的废液还可以重新使用。
【知识拓展】
(6)铁元素是维持生命活动不可缺少的微量元素,虽然人体中通常只含有3~5g铁元素,但铁元素在人体中却发挥着重要作用,人体缺铁会引起 疾病。
(13分)(1) 2Fe3+ + Cu = 2Fe2+ + Cu2+ [2分]
(2)0.1 [2分]
(3)KSCN溶液(或NaOH溶液), 溶液呈(血)红色(或红褐色沉淀) [每空2分(其它合理答案均得分)]
(4)铁粉 [2分]
(5)2FeCl2+Cl2=2FeCl3 [2分]
(6)贫血 [1分]
解析试题分析:(1)离子方程式的书写步骤一般为:①“写”:写出有关反应的化学方程式;②“拆”:可溶性的电解质用离子符号表示,其它难溶的物质、气体、水等仍用化学式表示;③“删”:删去方程式两边不参加反应的离子;④“查”:检查式子两边的各种原子的个数及电荷数是否相等.可根据反应原理及离子方程式的书写规律和要求进行分析解答。故离子方程式为2Fe3+ + Cu = 2Fe2+ + Cu2+。
(2)根据化学方程式计算,3.2g的铜即0.05mol,故至少需要FeCl3物质的量为0.1mol。
(3)Fe3+与KSCN溶液反应生成(血)红色物质,故试剂为KSCN溶液。现象为溶液呈(血)红色。
(4) 铁的活泼性大于铜,可以置换出铜,故加入的物质为铁粉。
(5)氯气的氧化性大于Fe2+的氧化性,反应氧化还原反应可以生成FeCl3,方程式为2FeCl2+Cl2=2FeCl3。
(6)缺少铁元素,人体会贫血。
考点:铁盐和亚铁盐的相互转变 离子方程式的书写
点评:本题考查学生铁及化合物的性质,可以根据所学知识进行回答,难度不大。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源: 题型:
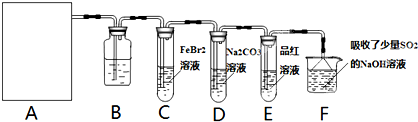
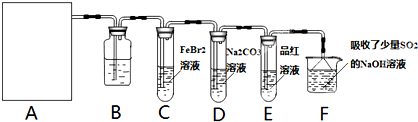
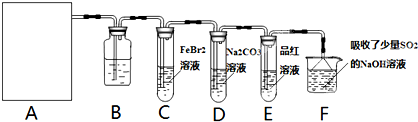
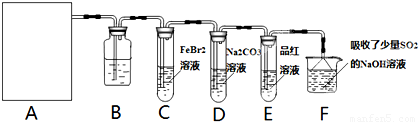
莫尔盐[(NH4)2SO4?FeSO4?6H2O]空气中比一般亚铁盐稳定,是化学分析中常用的还原剂。某研究性学习小组用下图所示的实验装置来制取莫尔盐,实验步骤如下:

① 用30%的NaOH溶液和废铁屑混合、煮沸、冷却、分离,将分离出的NaOH溶液装入F中;
② ②在E中用①处理过的铁屑和稀H2SO4反应制取FeSO4;
③ 将②制得的FeSO4溶液与(NH4)2SO4溶液混合,结晶得到莫尔盐。
试回答下列问题:
(1)利用铁屑和稀硫酸反应产生的氢气赶走装置中的氧气及硫酸铵溶液中溶解的氧,其目的是 ;铁屑和稀硫酸反应产生的氢气的另外一个作用是 。
(2)如何设计一个简单的实验证明得到的产品中有Fe2+?
。
(3)为了确定产品中亚铁离子的含量,研究小组用滴定法来测定。若取产品24.50g配成100mL溶液,取出10mL用0.10mol?L-1KMnO4酸性溶液滴定,消耗KMnO4溶液10.00mL。
①(2分)试配平反应的离子方程式:
MnO-4+ Fe2++ H+ == Fe3++ Mn2+ + H2O
②(4分)求产品中莫尔盐的质量分数 。(莫尔盐的相对分子质量为392)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省泸州市高级教育培训学校高三(上)月考化学试卷(10月份)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com