
二氧化碳是一种宝贵的碳氧资源。以CO2和NH3为原料合成尿素是固定和利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) NH2CO2NH4(s)??? △H1=a kJ·mol-1
NH2CO2NH4(s)??? △H1=a kJ·mol-1
反应Ⅱ:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g)??? △H2=+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g)??? △H2=+72.49kJ·mol-1
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)??? △H3=-86.98kJ·mol-1
CO(NH2)2(s)+H2O(g)??? △H3=-86.98kJ·mol-1
请回答下列问题:
(1)反应Ⅰ的△H1=__________kJ·mol-1(用具体数据表示)。
(2)反应Ⅱ的△S______(填>或<)0,一般在__________情况下有利于该反应的进行。
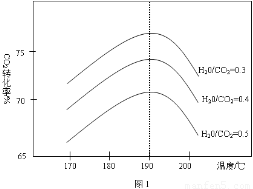
(3)反应Ⅲ中影响CO2平衡转化率的因素很多,下图1为某特定条件下,不同水碳比n(H2O)/n(CO2)和温度影响CO2平衡转化率变化的趋势曲线。
①其他条件相同时,为提高CO2的平衡转化率,生产中可以采取的措施是________(填提高或降低)水碳比。
②当温度高于190℃后,CO2平衡转化率出现如图1所示的变化趋势,其原因是__________。
(4)反应Ⅰ的平衡常数表达式K1=____________________;如果起始温度相同,反应Ⅰ由在恒温容器进行改为在绝热(与外界没有热量交换)容器中进行,平衡常数K1将__________(填增大、减少、不变)。
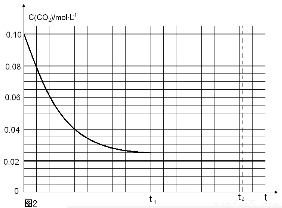
(5)某研究小组为探究反应Ⅰ中影响c(CO2)的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,t1时达到平衡过程中c(CO2)随时间t变化趋势曲线如上图2所示。若其他条件不变,t1时将容器体积压缩到1L,请画出t1后c(CO2)随时间t变化趋势曲线(t2达到新的平衡)。
(6)尿素在土壤中会发生反应CO(NH2)2+2H2O (NH4)2CO3。下列物质中与尿素有类似性质的是______。
(NH4)2CO3。下列物质中与尿素有类似性质的是______。
A.NH2COONH4B.H2NOCCH2CH2CONH2
C.HOCH2CH2OHD.HOCH2CH2NH2
(14分)(1)-159.47(2分)? (2)>(1分)? 高温(1分)
(3)①降低(1分)②温度高于190℃时,因为反应Ⅲ是放热反应,温度升高平衡向逆方向进行,CO2的平衡转化率降低,(2分,给出合理解释即可给分)。
(4)K1=1/[c2(NH3)·c(CO2)] (2分),减少(1分)
(5)
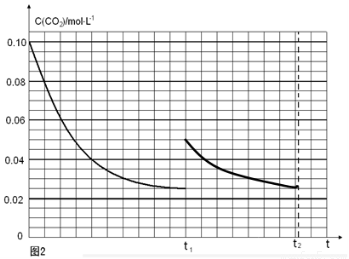 (注意:曲线的起点、平衡点和变化趋势共2分)
(注意:曲线的起点、平衡点和变化趋势共2分)
(6)A、B(2分)
【解析】
试题分析:解:(1)反应Ⅰ:2NH3(g)+CO2(g) NH2CO2NH4(s)△H1=a kJ·mol-1
NH2CO2NH4(s)△H1=a kJ·mol-1
反应Ⅱ:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g)△H2=+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g)△H2=+72.49kJ·mol-1
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)△H3=-86.98kJ·mol-1
CO(NH2)2(s)+H2O(g)△H3=-86.98kJ·mol-1
由盖斯定律总反应Ⅲ-反应Ⅱ,得到2NH3(g)+CO2(g) NH2CO2NH4(s)△H1=a=-159.47kJ·mol-1,
NH2CO2NH4(s)△H1=a=-159.47kJ·mol-1,
故答案为:-159.47;
(2)反应Ⅱ:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g)△H2=+72.49kJ?mol-1,反应前后气体体积增大,△S>0,焓变分析可知是吸热反应,△H>0,所以依据反应自发进行的判断依据△H-T△S<0,需要在高温下反应自发进行,故答案为:>;高温;
CO(NH2)2(s)+H2O(g)△H2=+72.49kJ?mol-1,反应前后气体体积增大,△S>0,焓变分析可知是吸热反应,△H>0,所以依据反应自发进行的判断依据△H-T△S<0,需要在高温下反应自发进行,故答案为:>;高温;
(3)①反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)△H3=-86.98kJ·mol-1,其他条件相同时,为提高CO2的平衡转化率,平衡正向进行,依据图象中的水碳比数据分析判断,生产中可以采取的措施是降低水碳比,二氧化碳转化率增大,故答案为:降低;
CO(NH2)2(s)+H2O(g)△H3=-86.98kJ·mol-1,其他条件相同时,为提高CO2的平衡转化率,平衡正向进行,依据图象中的水碳比数据分析判断,生产中可以采取的措施是降低水碳比,二氧化碳转化率增大,故答案为:降低;
②反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)△H3=-86.98kJ?mol-1,是放热反应,升温高于190℃,依据图象分析可知,二氧化碳转化率减小,因为温度升高,平衡逆向进行,
CO(NH2)2(s)+H2O(g)△H3=-86.98kJ?mol-1,是放热反应,升温高于190℃,依据图象分析可知,二氧化碳转化率减小,因为温度升高,平衡逆向进行,
故答案为:温度高于190℃时,因为反应Ⅲ是放热反应,温度升高平衡向逆方向进行,CO2的平衡转化率降低;
(4)反应Ⅰ:2NH3(g)+CO2(g) NH2CO2NH4(s)△H1=-159.47kJ?mol-1,平衡常数K=
NH2CO2NH4(s)△H1=-159.47kJ?mol-1,平衡常数K=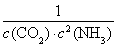 ;
;
起始温度相同,反应Ⅰ由在恒温容器进行改为在绝热(与外界没有热量交换)容器中进行,反应是放热反应,随反应进行温度升高平衡逆向进行,平衡常数减小;
(5)在恒温下将0.4mol NH3和0.2mol CO2放入容积为2L的密闭容器中,达到平衡时,
??????????????? 2NH3(g)+CO2(g) NH2CO2NH4(s)
NH2CO2NH4(s)
起始量(mol·L-1)? 0.2?????? 0.1?????????? 0
变化量(mol·L-1) 0.15?????? 0.075
平衡量(mol·L-1) 0.05??????? 0.025
t1时达到平衡过程中c(CO2)随时间t变化趋势曲线如图2所示.若其他条件不变,t1时将容器体积压缩到1L,二氧化碳浓度应增大到0.05mol·L-1,压强增大,平衡正向进行,由于生成物是固体,所以达到平衡状态,二氧化碳浓度保持不变,据此画出变化曲线为:
 ;
;
(6)尿素在土壤中会发生反应CO(NH2)2+2H2O (NH4)2CO3.分析结构特征可知,物质性质取决于官能团,尿素中氨基和羰基相连和水反应生成铵根离子,所以选项中符合此结果特征的有类似性质:
(NH4)2CO3.分析结构特征可知,物质性质取决于官能团,尿素中氨基和羰基相连和水反应生成铵根离子,所以选项中符合此结果特征的有类似性质:
A.NH2COONH4 ,结构中含有与羰基连接的氨基,故A符合;
B.H2NOCCH2CH2CONH2 结构中含有与羰基连接的氨基,故B符合;
C.HOCH2CH2OH,结构中不含有氨基,故C不符合;????????
D.HOCH2CH2NH2,分子中的氨基不是和羰基连接,不具备次性质,故D不符合;
故答案为:A、B。
考点:本题考查热化学方程式和盖斯定律的计算应用,化学平衡影响因素分析判断,平衡常数,图象绘制与分析。


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com