
下列各组原子中,彼此化学性质一定相似的是
A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
C.2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y原子
D.最外层都只有一个电子的X、Y原子
C
【解析】
试题分析:
A项,原子核外电子排布式1s2的X原子是稀有气体,原子核外电子排布式为1s22s2的Y原子是ⅡA族,化学性质不同;B项,原子核外M层上仅有两个电子的X原子是ⅡA主族的元素原子,而原子N层上仅有两个电子的Y原子可能是副族或Ⅷ族元素原子,故性质不一样;C项,2p轨道上只有2个电子的X原子是C原子,3p轨道上只有2个电子的Y原子是Si原子,两者化学性质相似;D项,最外层只有一个电子的原子可能是IA族元素原子,也可能是过渡金属原子,故化学性质不一定相同。
考点:原子核外电子排布与元素性质
点评:本题考查原子核外电子排布与元素性质,难度不大。需要熟悉几种常见元素原子的核外电子排布。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:填空题
(10分,每空2分)现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)取10 mL的甲溶液,加入等体积的水,醋酸的电离平衡________移动(填“向左”、“向右”或“不”);另取10 mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中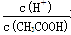 的比值将__________(填“增大”、“减小”或“无法确定”)。
的比值将__________(填“增大”、“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)________pH(乙)(填“大于”、“小于”或“等于”)。
(3)取25 mL的甲溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为:c(Na+)________c(CH3COO-)。(填“大于”、“小于”或“等于”)。
(4)室温下,现有pH=2的醋酸溶液与PH=12的氨水,等体积混合后,溶液呈中性,则溶液中离子浓度的大小关系:_______
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省东营市高一上学期第三次模块考试化学试卷(解析版) 题型:选择题
下列各组气体中,在通常条件下能稳定共存的是
A. NH3、HCl B. H2S、SO2 C. NO、O2 D. N2、O2
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二12月月考化学试卷(解析版) 题型:选择题
下面有关晶体的叙述中,不正确的是
A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二12月月考化学试卷(解析版) 题型:选择题
下列物质中存在配位键的是
①H3O+ ②[B(OH)4]- ③CH3COO- ④NH3 ⑤CH4
A.①② B.①③ C.④⑤ D.②④
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二12月月考化学试卷(解析版) 题型:选择题
某化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等)。下列物质中与该产品互为同分异构体的是

A.CH2===C(CH3)COOH
B.CH2===CHCOOCH3
C.CH3CH2CH===CHCOOH
D.CH3CH(CH3)COOH
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市闵行区高二第一学期期末考试化学试卷(解析版) 题型:填空题
(本题共10分)
某实验小组利用如下图装置,测定某种旧铝合金(含Al2O3和其它不溶于NaOH溶液的成分)中Al的质量分数,其中100mLNaOH溶液过量,每隔相同时间读得电子天平的数据如下表:

称量对象 | 读数次数 | 质量(g) |
样品 | 第1次 | 2.582 |
锥形瓶+100mL NaOH溶液 | 第2次 | 185.721 |
锥形瓶+NaOH溶液+样品 | 第3次 | 188. 286 |
第4次 | 188. 254 | |
第5次 | 188. 243 | |
第6次 | 188. 243 |
52.反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市闵行区高二第一学期期末考试化学试卷(解析版) 题型:填空题
a(g)镁和足量稀硫酸反应,镁完全反应后,测得氢气在常温时的体积为V(L),则常温下l mol氢气的体积为_________________L。
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期期末联考化学试卷(解析版) 题型:填空题
(6分)比较法是化学中研究物质性质的基本方法之一,请运用比较法解答下题。Na2O2几乎可与所有的常见气态非金属氧化物反应。如2Na2O2+2CO2 == 2Na2CO3+O2,Na2O2+CO= Na2CO3。
(1)通过比较可知,当非金属元素处于____________价时,其氧化物与Na2O2反应有O2生成。
(2)试分别写出Na2O2与SO2、SO3反应的化学方程式:_____________;_____________。
(3)氰(CN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素。试写出(CN)2与水反应的化学方程式:________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com