
| A. | 地沟油经过加工处理后,可以用来制肥皂和生物柴油 | |
| B. | PM2.5颗粒(微粒直径约为2.5×10-6m)分散在空气中形成气溶胶 | |
| C. | 采用纳米TiO2光触媒技术,可将装修材料中释放的HCHO转化为无害物质 | |
| D. | 神舟十一号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是硅晶体 |
分析 A.地沟油属于油脂,油脂可发生皂化反应制肥皂;生物柴油是以动植物油脂、废餐饮用油等为原料与甲醇在催化剂作用下,进行酯交换制成的液体燃料;
B.气溶胶属于胶体,微粒直径在10-7m~10-9m之间;
C.释放的HCHO转化为无害物质,减少对环境的污染;
D.硅是良好的半导体材料.
解答 解:A.地沟油经过皂化反应制肥皂,与甲醇在催化剂作用下进行酯交换制成生物柴油,故A正确;
B.PM2.5(微粒直径约为2.5×10-6m)微粒直径大于10-7m,不能形成气溶胶,故B错误;
C.释放的HCHO转化为无害物质,减少对环境的污染,则采用纳米TiO2光触媒技术将装修材料中释放的HCHO转化为无害物质合理,故C正确;
D.硅是良好的半导体材料,用于制造太阳能电池,故D正确;
故选B.
点评 本题综合考查物质的性质和用途,为高考常见题型,侧重于化学生产、生活的考查,有利于提高学生的环境保护意识,注意把握相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:实验题
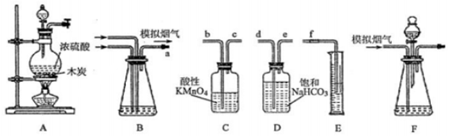
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

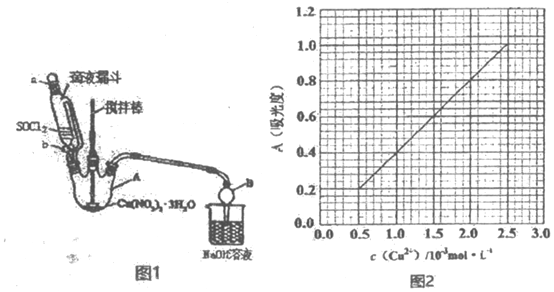
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光纤通信使用的光缆的主要成分是晶体Si,太阳能电池使用的材枓主要是SiO2 | |
| B. | 水玻璃可用作防火剂或防腐剂 | |
| C. | 高锰酸钾溶液、SO2、双氧水都能杀菌消毒,消毒原理相同,都利用了强氧化性 | |
| D. | SO2可用来漂白纸浆、毛、丝、草帽辫、增白食品等 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
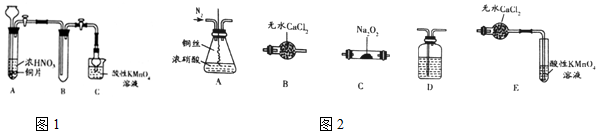
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “暖冰”中的水分子存在π键 | |
| B. | 水变成“暖冰”,体积会变小 | |
| C. | 在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” | |
| D. | -个水分子与其他水分子间只能形成2个氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 $→_{②H+}^{①浓KOH、△}$
$→_{②H+}^{①浓KOH、△}$ +
+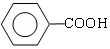
 .
. ,该反应的反应类型是缩聚反应.
,该反应的反应类型是缩聚反应. +4Ag(NH3)2++4OH-$\stackrel{△}{→}$
+4Ag(NH3)2++4OH-$\stackrel{△}{→}$ +2NH4++6NH3+4Ag↓+2H2O.
+2NH4++6NH3+4Ag↓+2H2O. 中任意一种.
中任意一种. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液除去锅炉中水垢(CaSO4):Ca2++CO32-═CaCO3↓ | |
| B. | 用惰性电极电解饱和硫酸铜溶液:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | 铝溶于氢氧化钠溶液:Al+2OH-+H2O=AlO2-+2H2↑ | |
| D. | 用H2O2从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com