
【题目】亚硝酰氯(NOC1)的沸点为-5.5℃,具有刺鼻恶臭味,在潮湿空气中易水解,溶于浓硫酸,是而机合成中的重要试剂。某同学用下图装置,由NO与干燥纯净的Cl2反应制备NOCl。
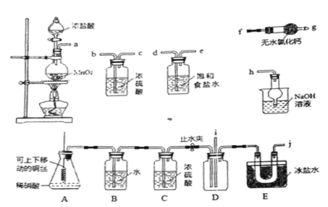
己知:①Cl2沸点为-34.6℃,NO2Cl沸点为-15℃
2NO+Cl2= 2NOC1 2NO2 + Cl2=2NO2C1
回答下列问题:
(1)铜与稀硝酸反应的化学方程式为_______________;装置A中设计了可上下移动的铜丝,其优点是_____________________。
(2)上图中实验装置的连接顺序为:a→_________________________。
(3)实验时,先制取氯气使充满除A、B、C外的整套装置,目的是__________________;
装置中充满氯气后,下—步是制取NO,具体操作是_______________________________;
E中冰盐水的温度可低至-22℃,其作用是________________________。
(4)该同学的实验设计可能的不足之处是________________________(答出一条即可)。
(5)若无C装置,则不利于NOCl的制备,主要原因是_________(用化学方程式表示)。
【答案】⑴ 3Cu + 8HNO3(稀)=3Cu(NO3)2+ 2NO↑+4H2O 可控制反应的开始和停止
⑵ d、e—b、c—i、j—f、g—h
⑶排出装置中的空气 打开止水夹,并将铜丝插入稀硝酸中 将NOCl冷凝为液态
⑷ B、C上部的空气会将NO氧化或:E中制得的NOCl产品中可能混有少量NO2Cl 。
⑸ NOCl + H2O= HNO2+HCl
【解析】(1)铜与稀硝酸反应生成硝酸铜和NO的化学方程式为3Cu + 8HNO3(稀)=3Cu(NO3)2+ 2NO↑+4H2O;装置A中可通过上下移动的铜丝,来控制反应的开始和停止;
(2)因亚硝酰氯易水解,制得的氯气需要干燥除杂,可通过饱和食盐水除去挥发的HCl,通过浓硫酸干燥,连接装置时要注意导管要长进短出,同时要注意尾气的处理,减小对环境的污染,实验装置的连接顺序为:a→d、e—b、c—i、j—f、g—h;
(3)NO遇空气中的氧气易氧化为NO2,则先制取氯气使充满除A、B、C外的整套装置可 排出装置中的空气;当装置中充满氯气后,打开止水夹,并将铜丝插入稀硝酸中,A装置中开始生成NO气体;亚硝酰氯(NOC1)的沸点为-5.5℃,易液化,E中冰盐水使温度降至-22℃,有利于NOCl冷凝为液态;
(4)B、C上部有空气,其中所含氧气将NO氧化为NO2,因2NO2 + Cl2=2NO2C1,则E中制得的NOCl产品中可能混有少量NO2Cl,这是实验设计存在的不足之处;
(5)若无C装置浓硫酸干燥NO,则NOCl在潮湿空气中易水解,发生NOCl + H2O= HNO2+HCl,不利于NOCl的制备。


科目:高中化学 来源: 题型:
【题目】外围电子排布式为3d104s1的元素在周期表中应位于( )
A. 第四周期ⅠB族 B. 第五周期ⅡB族
C. 第四周期ⅦB族 D. 第五周期ⅢB族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想将不溶的碳酸钙通过特殊的加工方法使之变为纳米碳酸钙(即碳酸钙粒子直径是纳米级),这将引起建筑材料的性能发生巨大变化,下列关于纳米碳酸钙的推测可能的是
A.纳米碳酸钙是与胶体相似的分散系
B.纳米碳酸钙分散到水中会产生丁达尔效应
C.纳米碳酸钙化学性质已与原来碳酸钙完全不同
D.纳米碳酸钙的粒子不能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量锌与浓H2SO4充分在加热下反应生成会SO2和H2的混合气体;锌和稀硫酸反应只有H2生成。现有甲乙两研究小组分别实验探究:
(1)甲研究小组按下图实验验证锌与浓硫酸反应生成物中SO2和H2,取少量的Zn置于b中,向a中加入100mL18.5mol·L-1的浓硫酸,经过一段时间反应,Zn完全溶解
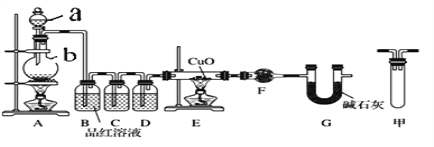
①填写仪器名称:a_____________、b_________。
②写出装置A中生成能使品红溶液褪色的化学反应方程式:_________________。
③装置D中加入的试剂是__________。
④U型管G的作用为______________。
⑤有同学认为A、B间应增加图中的甲装置,该装置的作用为__________。
⑥证明反应生成SO2和H2的实验现象是_________________。
⑦若A中生成标准状况下的气体33.6L,将A反应后的溶液稀释到1L,测得溶液中H+的浓度为0.1 mol·L-1,则稀释液中SO42-的物质的量浓度是_________ mol·L-1。
(2)乙研究小组为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。
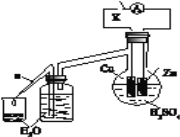
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是形成原电池反应速度快。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是_____________________________________。
③ 从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光导纤维被认为是20世纪最伟大的发明之一。2009年诺贝尔物理学奖获奖者英国华裔科学家高锟,在“有关光在纤维中的传输以用于光学通信方面”取得了突破性成就。光导纤维的主要成分是( )
A.Si
B.SiO2
C.Na2SiO3
D.SiCl4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com