
| A. | NH4Cl | B. | Na2CO3 | C. | CuSO4•5H2O | D. | [Co(NH3)6]Cl3 |
分析 分子或离子中若一种微粒提供空轨道,另一种微粒提供孤对电子,则形成配位键,据此分析.
解答 解:A.NH4Cl中NH4+的H+提供空轨道,N原子提供孤对电子,含有配位键,故A不选;
B.Na2CO3中没有空轨道,不能形成配位键,故B选;
C.CuSO4•5H2O中H2O含有孤电子对,Cu含有空轨道,含有配位键,故C不选;
D.[Co(NH3)6]Cl3中NH3含有孤电子对,Co含有空轨道,含有配位键,故D不选.
故选B.
点评 本题考查配位键的形成条件及其应用等,题目难度不大,需要学生全面掌握配位键的形成条件,并能运用分析解决问题,注意配位键形成的条件,一方要提供空轨道,另一方提供孤电子对.


科目:高中化学 来源: 题型:解答题
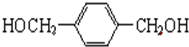 .
.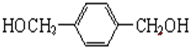 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$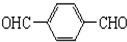 +2H2O.
+2H2O. .(原子量:Ag--108)
.(原子量:Ag--108)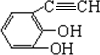 (只写出一种即可).
(只写出一种即可).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
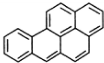 黄曲霉素、亚硝胺及3,4-苯并芘是世界公认的三大强烈致癌物质,3,4-苯并芘是一种稠环芳烃,其结构简式如图所示,则一氯3,4-苯并芘有( )
黄曲霉素、亚硝胺及3,4-苯并芘是世界公认的三大强烈致癌物质,3,4-苯并芘是一种稠环芳烃,其结构简式如图所示,则一氯3,4-苯并芘有( )| A. | 8种 | B. | 10种 | C. | 12种 | D. | 20种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
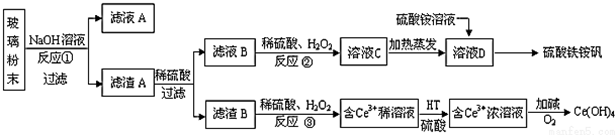
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
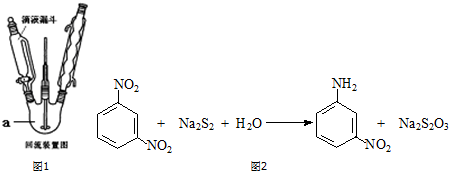
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-CH2CH2Cl | B. | (CH3)3CCH2OH | C. | CH3CHClCHO | D. | CH2=CHCH2COOCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com