
对下列各溶液中,微粒的物质的量浓度关系表述正确的是
A.0.1mol·L-1的(NH4)2CO3溶液中:c(CO32-)>c(NH4+)>c(H+)>c(OH-)
B. 0.1 mol·L-1的NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-)
C.将0.2 mol·L-1 NaA溶液和0.1 mol·L-1盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)
D.在25℃时,1mol·L-1的CH3COONa溶液中:c(OH-)=c(H+)+c(CH3COOH)
【知识点】溶液中的离子浓度关系 H3 H6
【答案解析】D 解析:A、0.1mol·L-1的(NH4)2CO3溶液中:c(NH4+)>c(CO32-),故A错误;B、0.1 mol·L-1的NaHCO3溶液中,根据物料守恒:c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-),故B错误;C、根据电荷守恒:c(Na+)+c(H+)=c(A-)+c(Cl-)+c(OH-),故C错误;D、根据质子守恒,溶液中水电离产生的氢氧根离子浓度一定等于水电离产生的氢离子浓度,故D正确。
故答案选D
【思路点拨】本题考查了溶液中的离子浓度关系,关键是理解并灵活应用电荷守恒、物料守恒、质子守恒。


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.糖类化合物都具有相同的官能团
B.酯类物质是形成水果香味的主要成分
C.油脂的皂化反应生成脂肪酸和丙醇
D.蛋白质的水解产物都含有羧基和羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
2008年北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”(Funiulele)。有一种有机物的键线式也酷似牛,故称为牛式二烯炔醇(cowenynenynol)。下列有关说法不正确的是( )
A.牛式二烯炔醇分子内含有两种官能团
B.牛式二烯炔醇能够发生加聚反应得到高分子化合物
C.牛式二烯炔醇在一定条件下能与乙酸发生酯化反应
D.牛式二烯炔醇可使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
某多肽的化学式为C42H65N11O9,它彻底水解后只得到以下三种氨基酸:甘氨酸H2N—CH2—COOH、苯丙氨酸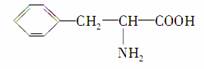 和赖氨酸
和赖氨酸
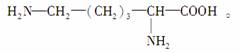
(1)该多肽为________肽(填汉字)。
(2)该多肽水解后能生成________个甘氨酸、______个苯丙氨酸、________个赖氨酸(填数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
从薄荷油中得到一种烃A(C10H16),叫α非兰烃,与A相关反应如下:
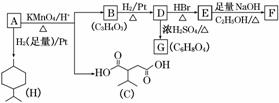
已知: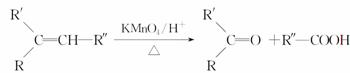
(1)H的分子式为________。
(2)B所含官能团的名称为________。
(3)含两个—COOCH3基团的C的同分异构体共有____________种(不考虑手性异构),其中核磁共振氢谱呈现2个吸收峰的异构体结构简式为___________________________。
(4)B→D,D→E的反应类型分别为________、________。
(5)G为含六元环的化合物,写出其结构简式: _____________________________。
(6)F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂名称为________。
(7)写出E→F的化学反应方程式: ________________________________________
________________________________________________________________________。
(8)A的结构简式为________,A与等物质的量的Br2进行加成反应的产物共有________种(不考虑立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列各图像的说法中正确的是
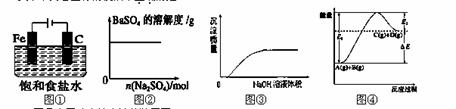
A.图①表示防止铁腐蚀的装置图
B.图②表示向BaSO4饱和溶液中加入硫酸钠
C.图③表示将NaOH溶液滴入Ba(HCO3)2溶液中
D.图④表示反应物的总键能大于生成物的总键能
查看答案和解析>>
科目:高中化学 来源: 题型:
结构简式为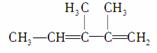 的化合物正确的命名是( )
的化合物正确的命名是( )
A.3,4二甲基2,3戊二烯 B.2,3二甲基2,4戊二烯
C.2,3二甲基1,3戊二烯 D.2,3二甲基2,3戊二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
.硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在 500℃时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和 。
(2)为检验分解产物的成份,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。
① A中固体充分加热较长时间后,通入氮气,目的是 。
②为验证A中残留物是否含有FeO,需要选用的试剂有 。
A.KSCN溶液 B.稀硫酸
C.浓盐酸 D.KMnO4溶液
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有 气体生成,若含有该气体,观察到的现象为 。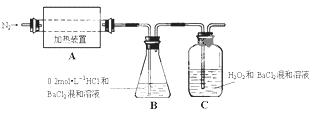
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则b a(填“大于”、“小于”或“等于”)
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应为
(用离子方程式表示)。
(3)已知亚铁离子被氧气氧化的反应是:4Fe2+ + O2 + (4+2x) H2O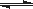 2Fe2O3•xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
2Fe2O3•xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com