
【题目】已知AJ 10种物质的转化关系如图所示:
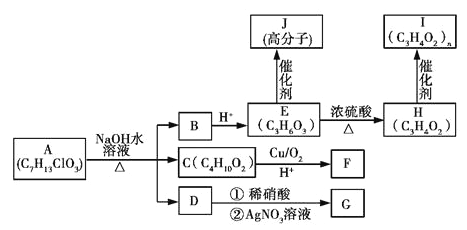
已知:①E分子中含有一个连有4个不同原子或原子团的碳原子。
②C分子中核磁共振氢谱中显示有四种不同的氢原子,且峰面积之比为4∶3∶2∶1。
③1 mol F与足量的新制氢氧化铜在加热条件下充分反应可生成2 mol砖红色沉淀。
④G为白色沉淀。
请回答下列问题:
(1)A中含有的含氧官能团的名称是______________。
(2)B的结构简式为__________________________。
(3)E生成H的化学方程式为_______________________________________。
(4)D的化学名称是__________________________________。
(5)高分子化合物J的结构简式为_______________________________。
(6)与C具有相同的官能团和相同的官能团数目,且官能团不在同一个碳原子上的C的同分异构体共有__________种,其中核磁共振氢谱有三种不同化学环境的氢原子,且峰面积之比为2∶2∶1的是________________________(写结构简式)。
【答案】 羟基、酯基 ![]()
![]()
![]() CH2—CHCOOH+H2O 氯化钠
CH2—CHCOOH+H2O 氯化钠 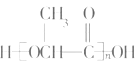
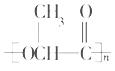 5 HOCH2CH2CH2CH2OH
5 HOCH2CH2CH2CH2OH
【解析】根据A的分子式和在NaOH溶液中反应生成B酸化后的E的分子式可知,E中含有羟基和羧基,根据A的分子式和在NaOH溶液中反应生成C的分子式可知,C为饱和二元醇,D能够与硝酸银溶液反应生成白色沉淀,可知D为NaCl,则A为含有Cl原子的酯,在NaOH溶液中发生卤代烃的水解和酯的水解,据E分子中含有一个连有4个不同原子或原子团的碳原子可知,E为CH3CHOHCOOH,B为CH3CHOHCOONa,据C分子中核磁共振氢谱中显示有四种不同的氢原子,且峰面积之比为4:3:2:1可知,C为HOCH2CH(CH3)CH2OH,则A为CH3CHClCOOCH2CH(CH3)CH2OH,E为CH3CHOHCOOH,能够通过酯化反应生成高分子化合物J,J为![]() ,E在浓硫酸作用下发生消去反应生成H,H为CH2=CHCOOH,H通过加聚反应生成I,I为
,E在浓硫酸作用下发生消去反应生成H,H为CH2=CHCOOH,H通过加聚反应生成I,I为![]() ,C为CH2OHCH(CH3)CH2OH,在Cu作催化剂时,催化氧化生成F,1mol F与足量的新制氢氧化铜在加热条件下充分反应可生成2mol红色沉淀,F为OHCCH(CH3)CHO;则
,C为CH2OHCH(CH3)CH2OH,在Cu作催化剂时,催化氧化生成F,1mol F与足量的新制氢氧化铜在加热条件下充分反应可生成2mol红色沉淀,F为OHCCH(CH3)CHO;则
(1)A为CH3CHClCOOCH2CH(CH3)CH2OH,其中含氧官能团有酯基、羟基;(2)据上述分析,B为CH3CHOHCOONa;(3)E为CH3CHOHCOOH,在浓硫酸作用下发生消去反应生成H,H为CH2=CHCOOH,反应方程式为:CH3CHOHCOOH![]() CH2=CHCOOH+H2O;(4)D能够与硝酸银溶液反应生成白色沉淀,可知D为NaCl;(5)E为CH3CHOHCOOH,能够通过酯化反应生成高分子化合物J,J为
CH2=CHCOOH+H2O;(4)D能够与硝酸银溶液反应生成白色沉淀,可知D为NaCl;(5)E为CH3CHOHCOOH,能够通过酯化反应生成高分子化合物J,J为![]() ;
;
(6)C为HOCH2CH(CH3)CH2OH,与C具有相同的官能团和相同的官能团数目,且官能团不在同一个碳原子上的C的同分异构体有:CH2OHCH2CH2CH2OH,CH2OHCHOHCH2CH3,CH2OHCH2CHOHCH3,CH3CHOHCHOHCH3,CH2OHC(CH3)OHCH3,共5种,其中核磁共振氢谱有三种不同化学环境的氢原子,且峰面积之比为2:2:1的是CH2OHCH2CH2CH2OH。


科目:高中化学 来源: 题型:
【题目】下列对分子的性质的解释中,不正确的是
A. 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致
B. 乳酸(![]() )有一对手性异构体,因为其分子中含有一个手性碳原子
)有一对手性异构体,因为其分子中含有一个手性碳原子
C. 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
D. 酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数比HClO的多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的钠铝合金置于水中,合金全部溶解,得到 20mL pH=14的溶液,然后用1 mol·L-1的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示:

写出有关反应的化学方程式:
(1)______________________________ ;(2)______________________________;
(3)______________________________ ;(4)____________________________ ;
(5)____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:

回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。
(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】位于短周期的四种元素A、B、C、D,它们的原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。回答下列问题:
(1)上述元素可以形成多种具有漂白性的物质,请写出任意两种物质的化学式:_________,______________;
(2)C与D形成D的最低价化合物的电子式:_________ ;
(3)写出C与水反应的离子方程式:______________________________;
(4)A、B组成的物质E可形成甲、乙两种微粒,它们均有10个电子。写出E生成甲、乙的方程式:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年冬季全国大部分地区出现雾霾现象,汽车尾气是造成雾霾的原因之一,汽车尾气含CO、NO等有毒气体。为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:
2CO(g)+O2(g)=2CO2(g); ΔH = -566kJ·moL-1
2H2(g)+O2(g)=2H2O(g); ΔH = -483.6KJ·moL-1
H2O (g)=H2O(l); ΔH = -44.0KJ·moL-1
(1)氢气燃烧热ΔH=__________;
(2)写出CO和H2O(g)作用生成CO2和H2的热化学方程式______________。
(3)往1L体积不变的容器中加入0.200mol CO和1.00mol H2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1(方程式中各物质前化学计量数为最简整数比),则t℃时CO的转化率为________;反应达到平衡后,升高温度,此时平衡常数将____(填“变大”、“不变”或“变小”)。
(4)从汽车尾气中分离出CO与O2、熔融盐Na2CO3组成的燃料电池,同时采用电解法制备N2O5,装置如图所示,其中Y为CO2。写出石墨I电极上发生反应的电极反应式_______________________________。在电解池中生成N2O5的电极反应式为__________________________________。

(5)在一定条件下,用NH3处理汽车尾气中的NO。已知NO与NH3发生反应生成N2和H2O,现有NO和NH3的混合物1mol,充分反应后得到的还原产物比氧化产物多1.4 g,则原反应混合物中NO的物质的量可能是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将以下4份溶液分别置于如图的装置中,其它条件相同时,灯泡最亮的是( )
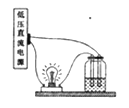
A. 80mL 1mol/L的NaCl溶液
B. 30mL 2mol/L的AlCl3溶液
C. 50mL 2mol/L的氨水
D. 60mL 2mol/L的蔗糖溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的结构如图所示,下列说法正确的是
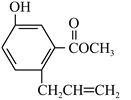
A. 1 mol X最多能与3 mol NaOH反应
B. X能与碳酸钠溶液产生二氧化碳
C. 1 mol X和浓溴水反应时,能消耗3 mol Br2
D. 1 mol X能最多能与5mol H2加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列叙述正确的是
A. a g C2H4和C3H6的混合物所含原子总数为![]()
B. 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
C. 标准状况下,22.4 L H2O含有的分子数为 NA
D. 物质的量浓度为0.5 mol·L1的MgCl2溶液中,含有Cl个数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com