
【题目】根据下图提供的信息,下列所得结论不正确的是
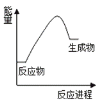
A. 该反应是吸热反应
B. 因为生成物的总能量高于反应物的总能量,所以该反应一定需要加热才能发生
C. 该反应反应物断裂旧键所吸收的能量高于生成物形成新键放出的能量
D. 该反应可能是碳酸钙分解反应
科目:高中化学 来源: 题型:
【题目】中国科学家用蘸墨汁书写后的纸张作为空气电极,设计并组装了轻型、柔性、能折叠的可充电锂空气电池如下左图,电池的工作原理如下右图。下列有关说法正确的是
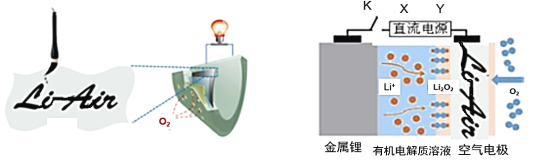
A. 放电时,纸张中的纤维素作为锂电池的负极
B. 充电时,若阳极放出1 mol O2,则有4 mol e-回到电源正极
C. 开关K闭合给锂电池充电,X为直流电源负极
D. 放电时,Li+由正极经过有机电解质溶液移向负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为H2与O2反应生成H2O(g)的能量变化示意图,下列有关叙述不正确的是

A. 1 mol H2分子断键需要吸收436 kJ的能量
B. H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ/mol
C. 反应物的总能量高于生成物的总能量
D. 形成化学键释放的总能量比断裂化学键吸收的总能量小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
一 | ① | |||||||
二 | ② | ③ | ④ | |||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
四 | ⑨ |
(1)在这些元素中,金属性最强的是________(填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是________。
(3)最高价氧化物是两性氧化物的元素是________;写出它的氧化物与氢氧化钠反应的离子方程式___________________________________________________________。
(4)③④⑤对应的简单离子半径由小到大的顺序为:______________。
(5)①与③可形成一种18 e- 的分子,写出该分子的电子式:__________,该分子中存在________(填“极性键”或“非极性键”或“离子键”)。
(6)①与⑤形成的化合物可与水反应生成一种无色气体,当转移0.5mol电子时,生成的气体在标准状况下的体积为______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示的实验,能达到实验目的的是
A | B | C | D |
|
|
|
|
验证化学能转化为电能 | 研究催化剂对化学反应速率的影响 | 实验室制氨气 | 验证非金属性:Cl>C>Si |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水资源开发利用的部分过程如下图所示(苦卤中主要含 K+、Mg2+、Br-等),下列说法错误的是
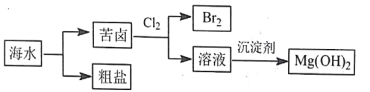
A. 从海水得到粗盐主要通过蒸发操作实现
B. 向苦卤中通入 Cl2 时溴离子被还原为 Br2
C. 富集溴涉及的离子反应有 Br2+SO2+2H2O==2Br-+4H++SO42-
D. 工业选用的沉淀剂通常经煅烧碳酸钙获得而不是电解食盐水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表示下列反应的离子方程式正确的是
A. 在强碱性溶液中次氯酸钠与 Fe(OH)3 反应生成 Na2FeO4: 3ClO3-+2Fe(OH)3 =2FeO42-+3Cl-+H2 O+4H+
B. 用浓盐酸与 MnO2 反应制取少量氯气:MnO2+2H++2Cl-= Mn2++Cl2↑+2H2O
C. 向 NaAlO2 溶液中通入过量 CO2 制 Al(OH)3:AlO2-+CO2+2H2O===Al(OH)3↓+HCO3-
D. 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-===3Fe3++NO2↑+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列判断正确的是

A. a为负极、b为正极
B. 电解过程中,c电极上发生氧化反应
C. d为阳极,电极反应为:2Cl―2e-=Cl2↑
D. 电解过程中,化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物中的所有原子可能都在同一平面上的是
A.CH3(CH2)4CH3B.CH3CH2CHO
C.CH2=CHCH=CH2D.(CH3)3C-C≡C-CH=CHCH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com