


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源:不详 题型:填空题
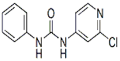
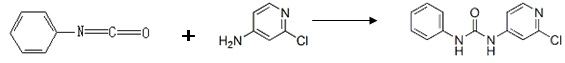
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O | 白色结晶粉末 | 170~172°C | 易溶于水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.随核电荷数递增,碱金属单质的熔沸点逐渐减小 |
| B.随核电荷数递增,碱金属单质的密度逐渐增大(Na、K反常) |
| C.碱金属元素包括F、Cl、Br、I、At五种元素 |
| D.碱金属元素的原子最外层都只有一个电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | | | | | ① | | ② | |
| 3 | | ③ | ④ | ⑤ | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | ⑩ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在化合物中呈+2价 | B.镭比钙的金属性强 |
| C.氢氧化物呈两性 | D.碳酸盐难溶于水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性强弱:HClO4>H2SO4>H3PO4 | B.离子半径:Na+>Mg2+>Al3+>F- |
| C.热稳定性:HCl>H2S>PH3>SiH4 | D.熔点:SiO2>NaCl>I2>CO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径 X>Y>Z | B.原子序数 X>Y>Z |
| C.气态氢化物稳定性 X<Y<Z | D.元素的非金属性 X<Y<Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com