
| A、标准状况下,22.4L氢气所含原子数是2NA |
| B、5.4g水所含的分子数为0.3NA |
| C、含1mol硫酸钾的溶液中硫酸根离子数为2NA |
| D、1mol金属钠与水反应失去的电子数为NA |


科目:高中化学 来源: 题型:
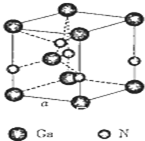 以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点.回答下列问题:
以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
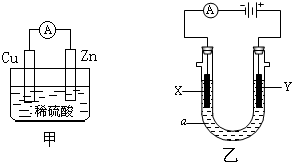 某化学兴趣小组的同学用如图装置研究电化学的问题.
某化学兴趣小组的同学用如图装置研究电化学的问题.查看答案和解析>>
科目:高中化学 来源: 题型:
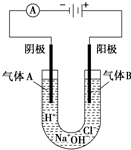 如图所示表示的是电解饱和食盐水的装置,阴极材料、阳极材料都是碳棒,饱和食盐水中含有少量酚酞.
如图所示表示的是电解饱和食盐水的装置,阴极材料、阳极材料都是碳棒,饱和食盐水中含有少量酚酞.查看答案和解析>>
科目:高中化学 来源: 题型:
283 116 |
| A、这种元素一定是金属元素 |
| B、它位于元素周期表中的第六周期 |
| C、这种原子的核外电子数为167 |
| D、这种元素的原子易与氢化合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Fe2O3+3CO
| ||||
| B、CO2+H2O═H2CO3 | ||||
C、CuO+H2
| ||||
D、2Na+O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打与氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O |
| B、向溴化亚铁溶液中通入少量的Cl2:Cl2+2Br-═2Cl-+Br2 |
| C、向新制氯水中滴加NaOH溶液后,黄绿色褪去:Cl2+2OH-═ClO-+Cl-+H2O |
| D、将鸡蛋壳浸泡在盐酸中:CaCO3+2H+═Ca2++CO2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| B、Na2O与盐酸反应:Na2O+2H+=2Na++H2O |
| C、向氢氧化钠溶液中通人过量C02:C02+OH-=HCO3- |
| D、钠与CuSO4溶液反应:2Na+Cu2+=2Na++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com