
【题目】氯气是一种重要的化工原料。工业上利用反应3Cl2 + 8NH3 = N2 + 6NH4Cl检查输送氯气的管道是否漏气。下列说法错误的是
A. 该反应属于置换反应 B. 该反应利用了Cl2的强氧化性
C. 生成1 mol N2时有6 mol电子转移 D. 若管道漏气遇氨就会产生白雾
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”、“偏小”或“无影响”)。
(4)实验中60 mL0.50 mol/L盐酸与50 mL0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”),简述理由:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学键的下列叙述中,下列叙述不正确的是
A.离子化合物可能含共价键 B.共价化合物不可能含离子键
C.离子化合物中一定含离子键 D.共价化合物中不含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解饱和食盐水可产生氯气、氢气和氢氧化钠,氯气与石灰乳反应可制漂白粉.
(1)请写出电解饱和食盐水的化学方程式.
(2)若电解饱和食盐水时消耗NaCl 58.5克,试计算理论上最多可得到氯气的体积(标准状况)?
(3)若将1mol氯气通入石灰乳中,理论上可得到次氯酸钙多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁片与稀硫酸反应制取氢气是,下列的措施中不能使氢气生成速率加快的是( )
A. 滴加少量硫酸铜溶液 B. 不用铁片,改用铁粉
C. 不用稀硫酸,改用98﹪浓硫酸 D. 加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是

A.原子半径:W >Z >X
B.非金属性:Z>Y
C.最高化合价:Z >X
D.最高价氧化物对应水化物的酸性:W>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,金属离子(Mn+)浓度的负对数值随溶液pH变化关系如图所示[已知:pM=-lgc(Mn+),且假设c(Mn+)≤10-6mol/L认为该金属离子已沉淀完全]。根据判断下列说法正确的是( )
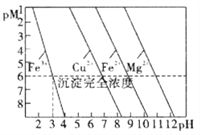
A. 常温下,Ksp[Mg(OH)2]<Ksp[Fe(OH)2]
B. 可以通过调节溶液pH的方法分步沉淀Cu2+和Fe2+
C. 除去Cu2+中少量Fe3+,可控制溶液3≤pH<4
D. pM与Ksp之间的关系式为:pM=lgKsp- nlgc(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个容积可变的密闭容器中发生反应:3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)。
Fe3O4(s)+4H2(g)。
回答下列问题:
(1)增加Fe的量,正反应速率 (填“增大”、“减小”或“不变”,下同)。
(2)将容器的容积缩小一半,正反应速率 ,逆反应速率 。
(3)保持容器的容积不变,充入N2使体系压强增大,正反应速率 ,逆反应速率 。
(4)保持压强不变,充入N2使容器的容积增大,正反应速率 ,逆反应速率 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 蛋白质的变性是可逆过程
B. 天然油脂没有恒定的熔点、沸点
C. 氨基乙酸不能溶于强酸溶液中
D. 蔗糖的水解产物不能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com