
 ;
; ;
;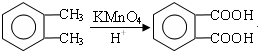 ;
; .(提示
.(提示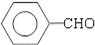 $\underset{\stackrel{①浓KOH、△}{→}}{②{H}^{+}}$
$\underset{\stackrel{①浓KOH、△}{→}}{②{H}^{+}}$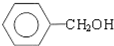 +
+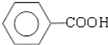 )
)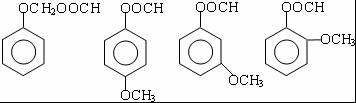 .
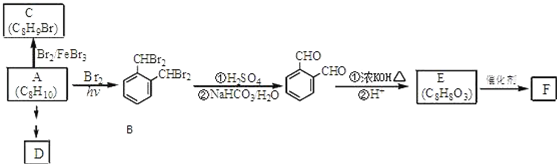
. 分析 A和溴发生取代反应生成B,根据B的结构简式知,A是邻二甲苯,在溴化铁作催化剂条件下,邻二甲苯和溴发生取代反应生成C ,B发生一系列反应后生成邻苯二甲醛,结合已知条件知,邻苯二甲醛反应生成E,E的结构简式为
,B发生一系列反应后生成邻苯二甲醛,结合已知条件知,邻苯二甲醛反应生成E,E的结构简式为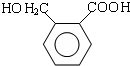 ,E发生缩聚反应生成F,F的结构简式为
,E发生缩聚反应生成F,F的结构简式为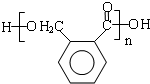 ,结合物质的性质来分析解答.
,结合物质的性质来分析解答.
解答 解:A和溴发生取代反应生成B,根据B的结构简式知,A是邻二甲苯,在溴化铁作催化剂条件下,邻二甲苯和溴发生取代反应生成C ,B发生一系列反应后生成邻苯二甲醛,结合已知条件知,邻苯二甲醛反应生成E,E的结构简式为
,B发生一系列反应后生成邻苯二甲醛,结合已知条件知,邻苯二甲醛反应生成E,E的结构简式为 ,E发生缩聚反应生成F,F的结构简式为
,E发生缩聚反应生成F,F的结构简式为 ,
,
(1)A的结构简式为: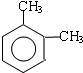 ,其名称是邻二甲苯,故答案为:邻二甲苯;
,其名称是邻二甲苯,故答案为:邻二甲苯;
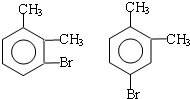
(2)邻二甲苯和溴发生取代反应生成B,邻二甲苯的甲基上氢原子被溴原子取代生成溴代烃,在该反应的副产物中,与B互为同分异构体的化合物的结构简式为 ,
,
故答案为:取代反应, ;
;
(3)在溴化铁作催化剂条件下,邻二甲苯和溴发生苯环上的取代反应,取代位置为甲基的邻、对位,所以C可能的结构简式为: ,
,
故答案为: ;
;
(4)酸性条件下,邻二甲苯被高锰酸钾氧化生成邻苯二甲酸,在浓硫酸、加热条件下,邻苯二甲酸和乙醇发生酯化反应生成邻苯二甲酸二乙酯,
故答案为: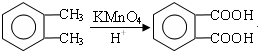
 ;
;
(5)OPA的化学名称是邻苯二甲醛,E发生缩聚反应生成F,该反应方程式为: ,
,
故答案为:邻苯二甲醛;缩聚反应; ;
;
(6)E的结构简式为 ,芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,则G的结构简式可能为:
,芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,则G的结构简式可能为: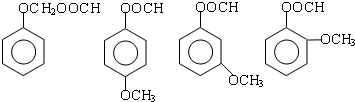 ,
,
故答案为: .
.
点评 本题考查有机物的推断,明确有机物的官能团及其性质是解本题关键,难度中等,难点是同分异构体的书写,注意不能多写、漏写.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:| 滴定次数 | 盐酸体积(ml) | NaOH溶液体积读数(ml) | |
| 滴定前 | 滴定后 | ||
| 20.00 | 0.00 | 16.30 | |
| 2 | 20.00 | 0.00 | 16.22 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
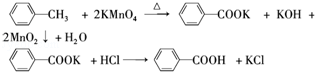
| 名称 | 相对分 子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |
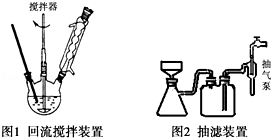
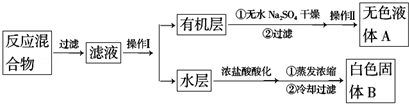
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B、C最简单氢化物的沸点依次递减,是因为A、B、C非金属性依次递减 | |
| B. | EB晶体是一种坚硬的高熔点材料,熔化时需克服离子键 | |
| C. | 在一定条件下,B的氧化物与B的简单氢化物均能反应生成单质B | |
| D. | C、D的常见氧化物均能溶于氢氧化钠溶液中,则C、D的氧化物均属于酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某温度下,1L pH=8的纯水中含OH-为10 -6mol | |
| B. | 电解精炼铜过程中,阳极质量的减少值与阴极质量的增加值一定相等 | |
| C. | 合成氨的反应是放热反应,则采用低温条件可以提高氨的生成速率 | |
| D. | CH3COOH溶液加水稀释后,溶液中$\frac{c(C{H}_{3}COOH)}{c(O{H}^{-})}$的值减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+ | B. | SO42- | C. | Ba2+ | D. | Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
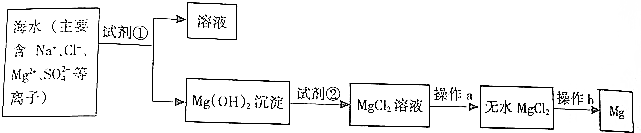
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com