
 某装置如图所示,该装置工作过程中,下列判断错误的是( )
某装置如图所示,该装置工作过程中,下列判断错误的是( )| 甲池 | 乙池 | |
| A | Zn极:Zn-2e-=Zn2+ | Cu极:Cu-2e-=Cu2+ |
| B | Cu2+移向C电极 | Cl-移向Fe电极 |
| C | 每消耗1mol Zn | 生成1mol气体 |
| D | C极的质量增加a g | Cu极的质量减小a g |
| A、A | B、B | C、C | D、D |


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
| 实验内容以及现象 | 结论 |
| ①取少量N溶液滴加足量的硝酸钡溶液,无沉淀产生 | N中不含 |
| ② |
确定M溶液中含有Na+,不含K+ |
③用pH试纸检测M溶液,pH试纸呈蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
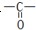 和C-OH两种原子团,A可能的结构简式为(写出一种即可)
和C-OH两种原子团,A可能的结构简式为(写出一种即可)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使pH试纸显蓝色的溶液中:Cu2+、NO3-、Fe3+、SO42- |
| B、与铝粉反应放出氢气的无色溶液中:NO3-、Al3+、Na+、SO42- |
| C、使红色石蕊试纸变蓝的溶液中:SO42-、CO32-、Na+、K+ |
| D、pH=0的溶液中:Al3+、NH4+、Ca2+、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱性溶液中:Na+、K+、SO32-、S2- |
| B、无色溶液中:Na+、Fe3+、Cl-、SO42- |
| C、无色溶液中:Na+、K+、HCO3-、AlO2- |
| D、酸性溶液中:Na+、K+、NO3-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2O2Cl4 |
| B、KCl?MgCl2?6H2O |
| C、KMnO4 |
| D、Cu2(OH)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9g重水(D2O)中所含质子数为0.5×6.02×1023 |
| B、电解精炼铜时,每转移l mol电子,阳极上溶解的金属必为32g |
| C、往存在V2O5的密闭容器中加入2molSO2和lmolO2,充分反应后分子总数等于2NA |
| D、VL a mol?L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.8g NH4+ 所含质子数为NA |
| B、通常状况下,NA个CO2分子占有的体积为22.4 L |
| C、物质的量浓度为0.5mol/L的BaCl2溶液中,含有Cl-个数为NA |
| D、1 mol?L-1的CaCl2溶液中,Cl-的物质的量浓度为2 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体都是均匀透明的液体 |
| B、直径介于1nm~100nm之间的微粒称为胶体 |
| C、胶体与溶液有明显不同的外观特征,呈胶状 |
| D、利用丁达尔效应可区别溶液和胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com