
【题目】(题文)(题文)PHB塑料是一种在微生物作用下可降解成无机物的环保型塑料,工业上可用异戊二烯合成:

已知:

(—R1、—R2、—R3、—R均为烃基)
请回答下列问题:
(1)A用系统命名法命名为_____,D中官能团的名称是_______。
(2)反应①的反应类型为_______________。
(3)B与H2反应后的产物的结构简式为![]() ,则B的结构简式为_____。
,则B的结构简式为_____。
(4)写出反应④的化学方程式:_________________________________。
(5)C的同分异构体X满足下列条件:
①能发生水解反应和银镜反应;②1个分子中含有2个碳氧双键。则符合条件的X共有______种。
另一种同分异构体Y能与碳酸钠溶液反应放出气体,能发生银镜反应,核磁共振氢谱共有四组峰且峰面积之比为1∶1∶2∶2,则Y的结构简式为_________。
(6)参照PHB的上述合成路线,设计一条由D为起始原料制备 的合成路线(其他试剂任选)______________。
的合成路线(其他试剂任选)______________。
【答案】2甲基1,3丁二烯羧基、羰基加成反应![]()
![]()
![]()
![]() +(n1)H2O7HOOCCH2CH2CHO
+(n1)H2O7HOOCCH2CH2CHO![]()
![]()
![]()
![]()
![]()
![]()

![]()
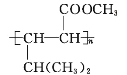
【解析】
(1)A为二烯烃,先确定双键的位置,再确定甲基的位置,根据系统命名法则进行命名;根据有机物D的结构简式,确定其含有的官能团。
(2)根据A的结构简式、B的分子式以及CH≡C-CH(CH3)2的分子式并结合已知①可判断出该反应类型。
(3) 由PHB的结构简式逆推可知E,再根据反应条件,逆推出C,再根据信息②,可以推出B的结构简式。
(4)由PHB的结构简式逆推可知E,通过分析PHB的结构,可知该高分子的生成是通过缩聚反应而实现的,据此写出反应方程式。
(5)有机物C的结构简式为CH3COCH2COOH,与它互为同分异构体,且满足①能发生水解反应和银镜反应,一定含有HCOO-结构;②1个分子中含有2个碳氧双键,根据分子式可知,结构含有-CO-结构,据此写出可能的结构简式;另一种同分异构体Y能与碳酸钠溶液反应放出气体,结构中含有羧基;能发生银镜反应,结构中含有醛基;核磁共振氢谱共有四组峰且峰面积之比为1∶1∶2∶2,据以上条件写出该有机物的结构简式。
(6)![]() 与H2先发生加成反应,再发生消去反应,然后与CH3OH发生酯化反应,最后发生加聚反应可得目标产物。据以上分析写出具体的流程图。
与H2先发生加成反应,再发生消去反应,然后与CH3OH发生酯化反应,最后发生加聚反应可得目标产物。据以上分析写出具体的流程图。
(1)A为烯烃,2号C原子上有一个—CH3,根据系统命名法则可知其名称为:2甲基1,3丁二烯;根据有机物D的结构简式可知,其含有的官能团为:羧基、羰基;正确答案:2甲基1,3丁二烯;羧基、羰基。
(2)比较A、B以及CH≡C-CH(CH3)2的分子式并结合已知①可知,反应①为加成反应;正确答案:加成反应。
(3)由PHB的结构简式逆推可知E为![]() ,再根据与氢气发生反应的条件,推知C为
,再根据与氢气发生反应的条件,推知C为![]() 。根据已知②,可得B的结构简式为
。根据已知②,可得B的结构简式为![]() ;正确答案:
;正确答案:![]() 。
。
(4)![]() 在一定条件下发生缩聚反应生成PHB,反应方程式如下:
在一定条件下发生缩聚反应生成PHB,反应方程式如下:![]()
![]()
![]() +(n1)H2O ;正确答案:
+(n1)H2O ;正确答案:![]()
![]()
![]() +(n1)H2O。
+(n1)H2O。
(5)有机物C的结构简式为CH3COCH2COOH,与它互为同分异构体,且满足①能发生水解反应和银镜反应,一定含有HCOO-结构;②1个分子中含有2个碳氧双键,含有-CO-;因此符合条件的X有7种:HCOOCH2COCH3、HCOOCOCH2CH3、HCOOCH2CH2CHO、![]() 、CH3CH2OOCCHO、CH3OOCCH2CHO、CH3COOCH2CHO;另一种同分异构体Y能与碳酸钠溶液反应放出气体,结构中含有羧基;能发生银镜反应,结构中含有醛基;核磁共振氢谱共有四组峰且峰面积之比为1∶1∶2∶2,符合条件下Y的结构简式为HOOCCH2CH2CHO;正确答案:7;HOOCCH2CH2CHO。
、CH3CH2OOCCHO、CH3OOCCH2CHO、CH3COOCH2CHO;另一种同分异构体Y能与碳酸钠溶液反应放出气体,结构中含有羧基;能发生银镜反应,结构中含有醛基;核磁共振氢谱共有四组峰且峰面积之比为1∶1∶2∶2,符合条件下Y的结构简式为HOOCCH2CH2CHO;正确答案:7;HOOCCH2CH2CHO。
(6)![]() 与H2先发生加成反应,再发生消去反应,然后与CH3OH发生酯化反应,最后发生加聚反应可得目标产物;具体流程如下:
与H2先发生加成反应,再发生消去反应,然后与CH3OH发生酯化反应,最后发生加聚反应可得目标产物;具体流程如下:![]()
![]()
![]()
![]()
![]()
![]()
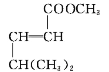
![]()
 ;正确答案:
;正确答案: ![]()
![]()
![]()
![]()
![]()
![]()
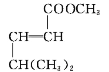
![]()
 。
。


科目:高中化学 来源: 题型:
【题目】波义耳在《怀疑的化学家》一书中说:“在火的单独作用下,玻璃容器的水银会丧失其原有的银色,变成一种红色物体;而无须使用任何附加试剂,用这种红色物体也可以得到汞”。 该过程可表示为"2Hg+O2![]() 2HgO”下列说法错误的是
2HgO”下列说法错误的是
A. 利用该反应可粗略测定空气中氧气的含量
B. 波义耳所描述的上述变化是一个可逆的化学反应
C. 水银温度计如果破损,可将硫粉洒在散落的水银上防止污染
D. 制备Hg单质可以采用热分解法使其氧化物在高温下分解制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝和铁是日常生活中两种常见的金属,铝和铁的化合物是中学化学中常见的基础物质。请回答下列有关问题:
(1)氧化铝是一种_____氧化物(填“酸性”“碱性”或“两性”);
(2)实验室制备氢氧化铝时,最好向铝盐溶液中加入_____。(填“氨水”或“氢氧化钠溶液”);
(3)还原铁粉与水蒸气反应的化学方程式为3Fe+4H2O(g) ![]() X+4H2,试推测X的化学式为_____。
X+4H2,试推测X的化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 100 g 质量分数为46%的乙醇(CH3CH2OH)水溶液中氧原子数为4NA
B. 标况下,46g NO2所含分子数目为NA
C. 1 mol Cl2通入足量NaOH溶液中,转移电子数为2NA
D. 0.5mol/L 的H2SO4溶液中,含有H+的个数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面叙述正确的是
A. 氯水应保存在无色的细口试剂瓶中
B. 液溴应保存在磨口玻璃塞的试剂瓶中,并加少量水进行水封
C. 能使湿润的淀粉碘化钾试纸变蓝的气体一定是氯气
D. 碘易溶于酒精,所以可以用酒精从碘水中萃取碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组采用刻蚀废液(主要含CuCl2、FeCl3、FeCl2、HCl)制取Cu和Cu2Cl2,实验流程如下:

已知:Cu2Cl2是白色固体,微溶于水,难溶于乙醇,受潮后在空气中易被迅速氧化。
(1)“预处理”时,需用Na2CO3调节溶液至微酸性而不是碱性,其原因是__________________。
(2)“还原Ⅰ”需在80 ℃条件下进行,适宜的加热方式为____________。
(3)“还原Ⅱ”中,Cu2+参与反应的离子方程式为__________________。
(4)“搅拌”时加入NaCl粉末的作用是____________________________。
(5)“过滤Ⅱ”得到的Cu2Cl2需用无水乙醇洗涤,并在真空干燥机内于70 ℃干燥2小时,冷却,密封包装。于70 ℃真空干燥的目的是__________________________。
(6)①设计从“过滤Ⅰ”所得滤渣中获取Cu的实验方案:稀硫酸加到滤渣中,搅拌,充分反应至无气体产生为止,过滤并用蒸馏水洗涤2~3次,低温烘干。
②现欲测定途径a、b回收铜元素的回收率比,请补充实验方案:____________________,分别按途径a、b制取Cu和Cu2Cl2,测得Cu的质量为m1 g,Cu2Cl2的质量为m2 g,则途径a、b铜元素的回收率比为________(铜元素回收率=产品中铜元素质量/废液中铜元素的质量×100%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对分别盛有不同无色溶液①②③④四支试管进行如下操作,现象和结论对应正确的是
操作 | 现象 | 结论 | |
A | 向①中先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
B | 向②(盛KI淀粉溶液)中通入少量的Cl2 | 溶液变蓝色 | Cl2与淀粉发生显色反应 |
C | 向③中溶液先滴加H2O2溶液,再滴加KSCN溶液 | 溶液变红色 | 原溶液中含有Fe2+ |
D | 向④中滴加浓NaOH溶液,加热,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 原溶液中有NH4+ |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,在强酸性和强碱性溶液中均能够大量共存的离子组是( )
A.NH4+、Cu2+、Cl-、NO3-B.K+、Na+、HCO3-、SO42-
C.Fe2+、NO3-、Na+、ClO-D.Cl-、NO3-、Na+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化锂是一种优良的贮氢材料,它是一种紫色或红色的晶状固体,在空气中长期暴露,最终会变成碳酸锂。氮化锂易水解生成氢氧化锂和氨气,在空气中加热能剧烈燃烧,特别是细粉末状的氮化锂;锂与氨反应生成LiNH2和H2。实验室用干燥、纯净的N2与金属锂(密度为0.534g·cm3)反应制取氮化锂。某课题组拟选择下列装置完成实验(装置可重复使用):

回答下列问题:
(1)若实验室用生石灰与浓氨水混合制备少量氨气,气流从左至右,选择上述装置制备少量氮化锂。装置连接顺序为__________________________________________。
(2)E装置的作用是_____________________________;写出D中化学方程式为______________________________。
(3)实验步骤如下:①装药品②引发反应产生氨气③检查装置气密性④点燃C处酒精灯⑤点燃D处酒精灯。正确的先后顺序为________________________________。(填序号)
(4)实验室保存锂的方法是______________;写出C中的化学方程式________________________________。氮化锂的电子式为_______________________________________
(5)设计简单实验证明C中产物为氮化锂:___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com