
 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )| A. | 在加热和催化剂作用下,最多能和4mol H2反应 | |
| B. | 不能使溴的CCl4溶液褪色 | |
| C. | 不能发生氧化反应 | |
| D. | 一定条件下,能与乙酸发生酯化反应 |
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2017年5月9日,中国科学院、国家语言文字工作委员会、全国科学技术名词审定委员会在京联合发布了115号等4个新合成元素的中文定名.115号定名为“镆”,在周期表中有关信息如右图所示,下列说法不正确的是( )
2017年5月9日,中国科学院、国家语言文字工作委员会、全国科学技术名词审定委员会在京联合发布了115号等4个新合成元素的中文定名.115号定名为“镆”,在周期表中有关信息如右图所示,下列说法不正确的是( )| A. | 该元素为金属元素,元素符号为“Mc” | |
| B. | 该元素为放射性元素 | |
| C. | 该元素原子核外电子数为115 | |
| D. | 该元素位于第七周期ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 通过传感器可以监测空气中甲醛的含量.一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是( )
通过传感器可以监测空气中甲醛的含量.一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是( )| A. | a为电池的正极,发生还原反应 | |
| B. | b极的电极反应为HCHO+H2O-4e-═CO2+4H+ | |
| C. | 传感器工作过程中,电解质溶液中硫酸的浓度减小 | |
| D. | 当电路中转移2×10-4 mol电子时,传感器内参加反应的HCHO为3.0 mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和乙烯互为同系物 | |
| B. | 葡萄糖和蔗糖不是同分异构体,但属于同系物 | |
| C. | 糖类、油脂、蛋白质都是由C、H、O三种元素组成的 | |
| D. | 油脂在酸性条件下水解为丙三醇和高级脂肪酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 结论 |
| A | 乙烯和苯都能使溴水褪色 | 苯和乙烯分子都含有碳碳双键 |
| B | 乙酸乙酯和乙烯一定条件下都能和水反应 | 两者属于同一类型的反应 |
| C | 乙酸和葡萄糖都能与新制的氢氧化铜反应 | 两者所含的官能团相同 |
| D | 乙烯能使溴的四氯化碳溶液和酸性高锰酸钾 溶液褪色 | 两者褪色的本质不相同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
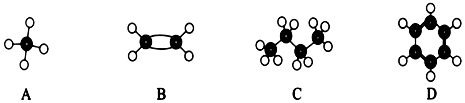
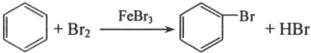 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,测定一定物质的量浓度的某NaA溶液的pH,pH>7,可以说明HA是弱酸 | |
| B. | 在一块镀锡铁板刻一划痕,滴加酸化的食盐水浸泡及KSCN溶液,溶液颜色没有变化,判断其具有好的耐腐蚀性 | |
| C. | 在氯化银的悬浊液中加入碘化钠溶液,沉淀颜色不变,说明氯化银的溶解度比碘化银大 | |
| D. | 在酸碱中和滴定中,用标准氢氧化钠溶液测定醋酸溶液的浓度时,用甲基橙做指示剂对滴定终点的判断比用酚酞的更准确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com