
| A. | 常温下,将铝片放入浓硫酸中,无明显现象,说明铝不与冷的浓硫酸反应 | |
| B. | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,说明浓氨水呈碱性 | |
| C. | H2S能与CuSO4溶液反应生成H2SO4,说明氢硫酸的酸性比硫酸强 | |
| D. | 向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,说明BaCl2有酸性 |
分析 A.常温下,浓硫酸和铝发生钝化现象;
B.碱能使红色石蕊试液变蓝色;
C.H2S能与CuSO4溶液发生复分解反应生成H2SO4;
D.Na2CO3和BaCl2反应生成碳酸钡沉淀,同时生成NaCl,溶液呈中性.
解答 解:A.常温下,浓硫酸和铝发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象是钝化现象而不是不反应,故A错误;
B.碱能使红色石蕊试液变蓝色,用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,则氨水中氢氧根离子浓度大于氢离子浓度,说明浓氨水呈碱性,故B正确;
C.H2S能与CuSO4溶液发生复分解反应生成H2SO4,但硫酸酸性大于硫化氢,故C错误;
D.Na2CO3和BaCl2反应生成碳酸钡沉淀,同时生成NaCl,溶液呈中性,导致溶液褪色,而不是氯化钡溶液呈酸性,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及钝化、溶液酸碱性判断等知识点,明确物质之间反应实质是解本题关键,易错选项是C.


科目:高中化学 来源: 题型:解答题

| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 废旧电池必须进行集中处理的主要原因是回收其中的碳电极 | |
| B. | 钠、镁等金属着火,可用CO2灭火 | |
| C. | “雨后彩虹”和“海市蜃楼”现象的出现与胶体的性质有关 | |
| D. | “加碘食盐”“含氟牙膏”“富硒营养品”“高钙牛奶”“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ①②④ | C. | ①②③ | D. | ②③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸的电子式  | B. | 钠离子的结构示意图 | ||
| C. | 硫原子的最外层电子排布式3s23p4 | D. | 二氧化硅的分子式 SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
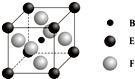 A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:
A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
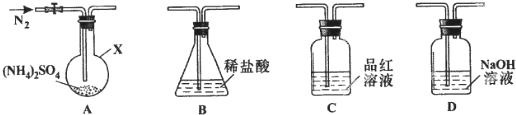
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液:Cu2+、Na+、NO3-、SO42- | |
| B. | 滴加紫色石蕊试液显红色的溶液:Fe2+、NH4+、Cl-、NO3- | |
| C. | 水电离出来的c(H+)=10-12mol/L的溶液:K+、Mg2+、SiO32-、Br- | |
| D. | 滴入KSCN显血红色的溶液中:Na+、Ba2+、Cl-、OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com