
��6�֣�X��Y��Z��RΪǰ������Ԫ�أ���ԭ��������������XY2�Ǻ���ɫ���壻X����Ԫ�ؿ��γ�XH3��Z��̬ԭ�ӵ�M����K���������ȣ�R2+���ӵ�3d�������9�����ӡ���ش��������⣺
��1��Y��̬ԭ�ӵĵ����Ų�ʽ�� ��
��2��R2+��ˮ�������У��ṩ�µ��ӶԵ�ԭ���� ��
��3��Z��ijԪ���γɵĻ�����ľ�������ͼ��ʾ���������������������ӵĸ������� ��
��4����R���ʵķ�ĩ����XH3��Ũ��Һ�У�ͨ��Y2����ַ�Ӧ����Һ������ɫ���÷�Ӧ�����ӷ���ʽ�� ��
��1��1s22s22p4 ;��2��O; ��3��2:1 ��4��2Cu+8NH3��H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O
��������
��������������������֪��X��N��Y��O��Z��Mg��R��Cu����1��O��̬ԭ�ӵĵ����Ų�ʽ��1s22s22p4 ; ��2��Cu2+��ˮ�������У��ṩ�µ��ӶԵ�ԭ����H2O�����е�Oԭ�ӣ���3�����ݾ����ṹʾ��ͼ��֪�������ӣ�1+8��1/8=2�������ӣ�4��1/2+2=4�����Ծ������������������ӵĸ�������4��2 = 2��1����40�������⣬��ϵ����غ㡢ԭ���غ�ɵ���Ӧ��Ӧ�����ӷ���ʽ��2Cu+8NH3��H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O��
���㣺����Ԫ�ص��ƶϡ�ԭ�ӽṹ�����ӽṹ������ṹ�����ӷ���ʽ����д��֪ʶ��


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д� ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������ʡ�߶����ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Ӧ��A B + C �������²����Է����У��ڸ��������Է����У��Ը÷�Ӧ���̡�H����S���ж���ȷ���ǣ� ��
B + C �������²����Է����У��ڸ��������Է����У��Ը÷�Ӧ���̡�H����S���ж���ȷ���ǣ� ��
A����H��0����S��0 B����H��0����S��0
C����H��0����S��0 D����H��������S��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������������ϸ���ѧ�߶���㿼�Ի�ѧ��A�ࣩ�Ծ��������棩 ���ͣ�ѡ����
��pH=4������X L�ֱ�������������Һ��Ϻ��Һ�������ԣ�
��1��10-4 mol/L�İ�ˮY L ��c(OH-)=1��10-4mol/L�İ�ˮZ L ��c(OH��)=1��10-4 mol/L��Ba(OH)2��ҺW L�� ����X��Y��Z��W�Ĺ�ϵ��ȷ����(����)
A��Y��X=W��Z B��X=Y��Z��W C��X=Y��W��Z D��Z��X=W��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭�ս�����һ������ѧϰ��������ѧ��⣩��ѧ�Ծ��������棩 ���ͣ�ѡ����
���б�ʾ�����У��������
A��2mol�� B��1molH2O C��4mole- D��0.5molH2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭�ս�����һ������ѧϰ��������ѧ��⣩��ѧ�Ծ��������棩 ���ͣ�ѡ����
���й�˵���У���ȷ����
A�����ʵ����������ʵ����� B��Ħ����һ��������
C��Ħ�������ʵ����ĵ�λ D��Ħ��������һ�ֺܴ�ĵ�λ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ���Ȼ�菉���ľ�������֪������2�������Cl- ���Ӻ˼��Ϊa cm���Ȼ�蘆�Ħ������ΪM g��mol��NAΪ�����ӵ����������Ȼ�菉�����ܶ�Ϊ�� ��
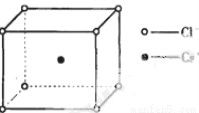
A��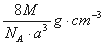 B��
B��
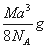
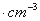
C�� 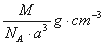 D��
D�� 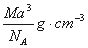
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������֣�ֻ��þ������̼����Ԫ�صľ��徹ȻҲ���г����ԣ���������Ԫ�ض��dz���Ԫ�أ��Ӷ�����㷺��ע�������ͳ��������һ��������ͼ��ʾ����þ���Ļ�ѧʽΪ
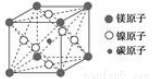
A��Mg2CNi3 B��MgCNi3 C��MgCNi2D��MgC2Ni
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
(6��) ��һ���¶���,��4mol SO2��2molO2����4L���ܱ������У���һ�������·�Ӧ��10����ʱ�ﵽƽ�⣺ 2SO2 + O2  2SO3 ���ƽ��ʱ����������ʵ���Ϊ5mol����
2SO3 ���ƽ��ʱ����������ʵ���Ϊ5mol����
��1��10����ʱO2�ķ�Ӧ����Ϊ mol/(L��min)��2��ƽ��ʱSO2��ת����
(3) ƽ�ⳣ��KΪ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ�������й���������ȷ����(����)
A����״���£�1L������ȫȼ�������ɵ���̬����ķ�����Ϊ7/22��4NA
B�� 1mol��(-CH3)�����ĵ�������Ϊ9NA
C�� 0��5mol 1, 3-����ϩ�����к���̼̼˫����ΪNA
D�� 1 mol��������ˮ������Ӧת�Ƶ��ӵ����ʵ���С��1mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com