
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1��ȡ����������Ʒ���Թ��У���������ˮ�������ܽ⣮ | �õ���ɫ��Һ |
| ����2�����Թ��м��������BaCl2��Һ�����ã� | ��Һ����ǣ���֤�������к��У�NH4��2CO3�� |
| ����3��ȡ����2���ϲ���Һ���Թ��м���������Ba��OH��2��Һ�� | ��Һ������ǣ���֤�������в�����NH4HCO3�� |
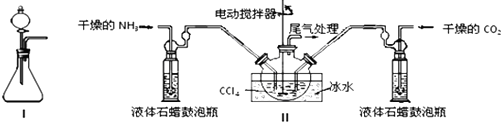
���� ��1��װ��1�����÷�Һ©������Һ���ܽ���ƿ�еĹ��壬�����ܽ����ʹ��ˮ�ֽ����ɰ�����
��2��������Ϊ��Һ©������Ӧ�Ƿ��ȷ�Ӧ����ƽ��������У�Һ��ʯ������ƿ����Ҫ�����ǿ��Ʒ�Ӧ���г̶ȣ������������ٺ�ԭ���������ȣ�
�����ɵİ��������С�������������Ȼ�̼�У������Ʒ��ʵ�鷽�����ù��˵õ�����������泥�NH2COONH4����һ�ְ�ɫ���壬�ֽ⣻
��3���ٸ���ʵ��Ŀ�ģ����鰱������刺��ܺ���̼����李�̼����е�һ�ֻ����֣�ͨ�����Թ��м��������BaCl2��Һ��������Һ����ǣ�֤�������к�̼��泥�Ȼ�����Թ��м�������Ba��OH��2��Һ������Һ�Ƿ�����֤���������Ƿ���̼����泥�
��̼����淋İ����������Ʒ�У�ʹ̼Ԫ����ȫת��Ϊ̼��ƣ�����̼Ԫ���غ�ͻ���������������ʵ���������
��� �⣺��1����Ũ��ˮ���뵽���������ƻ��������ƻ��ʯ�ң����ܽ�����з���ʹŨ��ˮ�ֽ����ɰ�����
�ʴ�Ϊ���������ƹ��壨��Ũ��ˮ���ʯ�һ�Ũ��ˮ����ʯ�ң��ȣ�
��2���ٸ�����������Ϊ��Һ©������Ӧ2NH3��g��+CO2��g��?NH2COONH4��s��+Q���Ƿ��ȷ�Ӧ������ƽ��������У��¶����ߣ��������ñ�ˮ��ȴ��߷�Ӧ����ת���ʣ���ֹ�������¶ȹ��߷ֽ⣻Һ��ʯ������ƿ�������ǿ��Ʒ�Ӧ���г̶ȣ������������ٺ�ԭ���������ȣ���ͨ���۲����ݣ�����NH3��CO2�ķ�Ӧ���ʣ���
�ʴ�Ϊ����Һ©����ͨ���۲����ݣ�����NH3��CO2ͨ���������ͨ���۲����ݣ�����NH3��CO2�ķ�Ӧ���ʣ��������¶ȣ���߷�Ӧ��ת���ʣ����¶ȣ���ֹ��Ӧ������ɲ���ֽ⣩��
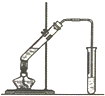
���Ʊ���������淋�װ����ͼ3��ʾ���Ѱ����Ͷ�����̼ͨ�����Ȼ�̼�У����Ͻ����ϣ����ɵİ��������С�������������Ȼ�̼�У������Ʒ��ʵ�鷽�����ù��˵õ�����������泥�NH2COONH4����һ�ְ�ɫ���壬�ֽ⡢���ܼ��Ⱥ�ɣ�Ӧ�����40�����º�ɣ�
�ʴ𰸣����ˣ�b��
��3���ٸ���ʵ��Ŀ�ģ����鰱������刺��ܺ���̼����李�̼����е�һ�ֻ����֣�ͨ�����Թ��м��������BaCl2��Һ��������Һ����ǣ�֤�������в���̼��泥��ڲ���̼��淋Ļ�������ͨ�����Թ��м�������Ba��OH��2��Һ������Һ�Ƿ�����֤���������Ƿ���̼����泥�
�ʴ�Ϊ��
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����2 | ��NH4��2CO3 |
| ����3 Ba��OH��2��Һ | NH4HCO3 |
���� ���⿼���������Ʊ�ʵ������Ӧ�ã�Ϊ�߿��������ͣ���Ŀ�漰�������Ʊ�����������������Ʊ�ʵ��װ�÷����жϣ�ʵ��������������������ʵ����ƣ��йػ����ļ��㣬��Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��������һ��һ��10���¿���ѧa���������棩 ���ͣ�ѡ����
�ס��ҡ��������ֱ���Na2CO3��AgNO3��BaCl2������������ɫ��Һ�е�һ�֣�����������Ӧ����������£��ף��ҡ��������ף������������ң�������������ʮ�����������ң�������ɫ��ζ���塣��ס��ҡ�������������Һ������
A��BaCl2��Na2CO3�����ᡢAgNO3
B��Na2CO3�����ᡢAgNO3��BaCl2
C��BaCl2��Na2CO3��AgNO3������
D��AgNO3�����ᡢBaCl2��Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
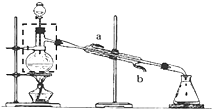 ijʵ��С������ˮ�Ҵ���������Ũ������ȡ�����������ᴿ����֪�Ҵ����Ժ��Ȼ��Ʒ�Ӧ�����ܵ�CaCl2•6C2H5OH����ش��������⣺
ijʵ��С������ˮ�Ҵ���������Ũ������ȡ�����������ᴿ����֪�Ҵ����Ժ��Ȼ��Ʒ�Ӧ�����ܵ�CaCl2•6C2H5OH����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ϩ��ʯ���ѽ�������Ҫ�ɷ֣���ϩ�Ľṹ��ʽΪH2C=CH2��
����ϩ��ʯ���ѽ�������Ҫ�ɷ֣���ϩ�Ľṹ��ʽΪH2C=CH2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
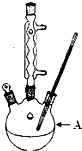 ������㷺Ӧ������ҩ�ͻ�����ҵ��ij��ȤС��ͬѧ���ø�����������ױ��Ʊ������ᣨKMnO4���������»�ԭ����ΪMnO2������������ΪMn2+��
������㷺Ӧ������ҩ�ͻ�����ҵ��ij��ȤС��ͬѧ���ø�����������ױ��Ʊ������ᣨKMnO4���������»�ԭ����ΪMnO2������������ΪMn2+��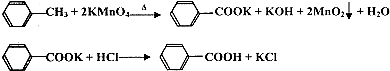
| ��һ�� | �ڶ��� | ������ | ���Ĵ� | |
| �����mL�� | 24.00 | 24.10 | 22.40 | 23.90 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
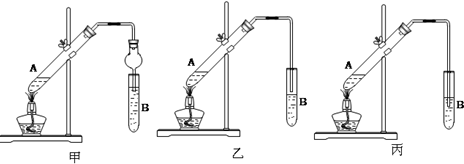
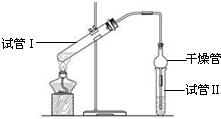 ������������Ҫ���л��ϳ��м��壬�㷺Ӧ���ڻ�ѧ��ҵ��ʵ����������ͼ��װ���Ʊ�����������
������������Ҫ���л��ϳ��м��壬�㷺Ӧ���ڻ�ѧ��ҵ��ʵ����������ͼ��װ���Ʊ�����������| ʵ���� | �Թܢ����Լ� | �Թܢ����Լ� | �л���� ���/cm |
| A | 2mL�Ҵ���1mL���ᡢ 1mL18mol•L-1 Ũ���� | ����Na2CO3 ��Һ | 3.0 |
| B | 2mL�Ҵ���1mL���� | 0.1 | |
| C | 2mL�Ҵ���1mL���ᡢ 3mL 2mol•L-1 H2SO4 | 0.6 | |
| D | 2mL�Ҵ���1mL���ᡢ���� | 0.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 | ����ֱ��/nm | ������H2O�Ľ����E/kJ•mol-1 |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com