(1)据报道以硼氢化合物NaBH
4(H的化合价为-1价)和H
2O
2作原料的燃料电池,可用作通信卫星电源.负极材料采用Pt/C,正极材料采用MnO
2,其工作原理如图1所示.写出该电池放电时负极的电极反应式:

(2)火箭发射常以液态肼(N
2H
4)为燃料,液态过氧化氢为助燃剂.
已知:N
2H
4(l)+O
2(g)=N
2(g)+2H
2O(l)△H=-534kJ?mol
-1H
2O
2(l)=H
2O(l)+
O
2(g)△H=-98.6kJ?mol
-1写出常温下,N
2H
4(l) 与 H
2O
2(l)反应生成N
2和H
2O的热化学方程式
.
(3)O
3可由臭氧发生器(原理如右图2所示)电解稀硫酸制得.
①图中阴极为
(填“A”或“B”).
②若C处通入O
2,则A极的电极反应式为:
(4)向一密闭容器中充入一定量一氧化碳跟水蒸气发生反应 CO(g)+H
2O(g)═CO
2(g)+H
2(g),下列情况下能判断该反应一定达到平衡状态的是
(选填编号).
A.v
正(H
2O)=v
逆(H
2)
B.容器中气体的压强不再发生改变
C.H
2O的体积分数不再改变
D.容器中CO
2和H
2的物质的量之比不再发生改变
E.容器中气体的密度不再发生改变
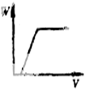
(5)温度T
1时,在一体积为2L的密闭容积中,加入0.4molCO
2和0.4mol的H
2,反应中c(H
2O)的变化情况如图3所示,T
1时反应CO(g)+H
2O(g)═CO
2(g)+H
2(g)第4分钟达到平衡.在第5分钟时向体系中同时再充入0.1molCO和0.1molH
2(其他条件不变),请在右图中画出第5分钟到9分钟c(H
2O)浓度变化趋势的曲线.



 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案