
| A£® | ¢Ł¢Ś¢Ū¢Ü¢Ż | B£® | Ö»ÓŠ¢Ł¢Ś¢Ü | C£® | Ö»ÓŠ¢Ł¢Ū¢Ż | D£® | Ö»ÓŠ¢Ł¢Ü |
·ÖĪö ¢Ł¶žŃõ»ÆĮņŗĶĖ®·“Ӧɜ³ÉŃĒĮņĖį£¬ŃĒĮņĖįŗĶŃõĘų·“Ӧɜ³ÉĮņĖį£»
¢Ś°±ĘųÓėŃõĘų·“Ó¦Ö»ÄÜÉś³ÉNO£¬²»ÄÜŅ»²½Éś³É¶žŃõ»ÆµŖ£»
¢ŪĀČ»ÆøĘÓė¶žŃõ»ÆĢ¼²»·“Ó¦£»
¢ÜĀČ»ÆĀĮÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘ£¬Ę«ĀĮĖįÄĘČÜŅŗĶØČė¶žŃõ»ÆĢ¼£¬Éś³ÉĒāŃõ»ÆĀĮ£»
¢ŻŃõ»ÆĶ²»ČÜÓŚĖ®£®
½ā“š ½ā£ŗ¢Ł¶žŃõ»ÆĮņŗĶĖ®·“Ó¦SO2+H2O?H2SO3£¬ŃĒĮņĖįŗĶŃõĘų·“Ó¦2H2SO3+O2ØT2H2SO4£¬¹Ź¢ŁÕżČ·£»
¢Ś°±ĘųÓėŃõĘų·“Ó¦Ö»ÄÜÉś³ÉNO£¬²»ÄÜŅ»²½Éś³É¶žŃõ»ÆµŖ£¬¹Ź¢Ś“ķĪó£»
¢ŪĀČ»ÆøĘÓė¶žŃõ»ÆĢ¼²»·“Ó¦£¬¹Ź¢Ū“ķĪó£»
¢ÜĀČ»ÆĀĮÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘ£¬Ę«ĀĮĖįÄĘČÜŅŗĶØČė¶žŃõ»ÆĢ¼£¬Éś³ÉĒāŃõ»ÆĀĮ£¬¹Ź¢ÜÕżČ·£»
¢ŻŃõ»ÆĶ²»ČÜÓŚĖ®£¬¹Ź¢Ż“ķĪó£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌŖĖŲ»ÆŗĻĪļµÄŠŌÖŹ£¬ŹģĻ¤Ļą¹ŲµÄ»Æѧ·“Ó¦µÄ·½³ĢŹ½ŹĒ½ā“šµÄ¹Ų¼ü£¬ĢāÄæ½Ļ¼ņµ„£®


 »ĘøŌ““ÓžķĻµĮŠ“š°ø
»ĘøŌ““ÓžķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
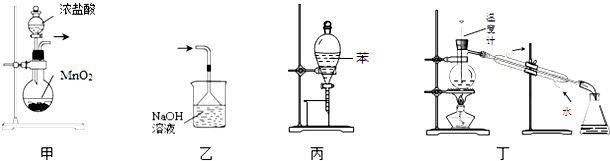
| A£® | ÓĆ×°ÖĆ¼×ÖĘČ”ĀČĘų | B£® | ÓĆŅŅ×°ÖĆ³żČ„ĀČĘųÖŠµÄHClĘųĢå | ||
| C£® | ÓƱū×°ÖĆŻĶČ”äåĖ®ÖŠµÄäåµ„ÖŹ | D£® | Óƶ”×°ÖĆ·ÖĄėŅŅĖįÓėŅŅ“¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Čō1molSO2ŗĶ1molO2³ä·Ö·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ2”Į6.02”Į1023 | |
| B£® | ŌŚøÖĢś±ķĆęĶæĖ¢ŗ¬ĀĮ·ŪµÄ·ĄŠāĘį£¬æÉŅŌÓŠŠ§·ĄÖ¹øÖĢśøÆŹ“ | |
| C£® | ŌŚŹŅĪĀĻĀ£¬Ļņ“×ĖįČÜŅŗÖŠ²»¶ĻĶØČėNH3£¬$\frac{c£ØC{H}_{3}COOH£©}{c£Ø{H}^{+}£©}$²»¶Ļ¼õŠ” | |
| D£® | ŹŅĪĀĻĀ£¬·“Ó¦Cl2£Øg£©+H2O£Øl£©ØTHCl£Øaq£©+HClO£Øaq£© ÄÜ×Ō·¢½ųŠŠ£¬Ōņ”÷H£¾0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĖÄĀČ»ÆĢ¼·Ö×ӵıȥżÄ£ŠĶ£ŗ | |
| B£® | ōĒ»łæÉŅŌ±ķŹ¾ĪŖ£ŗ-OH »ņ 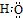 | |
| C£® | ĀČĄė×Ó£ØCl-£©µÄ½į¹¹Ź¾ŅāĶ¼£ŗ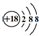 | |
| D£® | NaHSO4ČŪČŚŹ±µÄµēĄė·½³ĢŹ½£ŗNaHSO4=Na++H++SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 0.1 mol•L-1 CH3COONaČÜŅŗÓė0.1 mol•L-1 CaCl2ČÜŅŗµČĢå»ż»ģŗĻ£ŗc£ØNa+£©+2c£ØCa2+£©=c£ØCH3COO-£©+c£ØCH3COOH£©+c£ØCl-£© | |
| B£® | ÅØ¶Č¾łĪŖ0.1 mol•L-1µÄŠ”ĖÕ“ņČÜŅŗÓėÉÕ¼īČÜŅŗµČĢå»ż»ģŗĻ£ŗc£ØOH-£©-c£ØH+£©=c£ØHCO3-£©+c£ØH2CO3£© | |
| C£® | pHĻąĶ¬µÄ°±Ė®”¢KOHČÜŅŗ”¢Ba£ØOH£©2ČÜŅŗÖŠ£ŗc£ØNH4+£©=c£ØK+£©=2c£ØBa2+£© | |
| D£® | ³£ĪĀĻĀ£¬0.2 mol•L-1 NH4NO3ČÜŅŗÓė0.1 mol•L-1 NaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆpH=9.6µÄČÜŅŗÖŠ£ŗc£ØNO3-£©£¾c£ØNa+£©£¾c£ØNH4+£©£¾c£ØNH3•H2O£©£¾c£ØOH-£©£¾c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
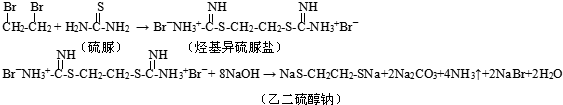
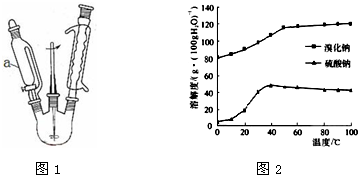
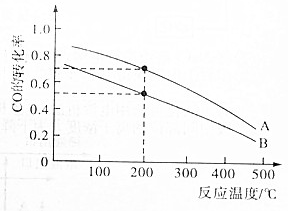 øßĀÆĮ¶Ģś²śÉśµÄ·ĻĘųÖŠµÄCOæɽųŠŠ»ŲŹÕ£¬Ź¹ĘäŌŚŅ»¶ØĢõ¼žĻĀŗĶH2·“Ó¦Öʱø¼×“¼£ŗCO£Øg£©+2H2£Øg£©?CH3OH£Øg£©£®Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£®
øßĀÆĮ¶Ģś²śÉśµÄ·ĻĘųÖŠµÄCOæɽųŠŠ»ŲŹÕ£¬Ź¹ĘäŌŚŅ»¶ØĢõ¼žĻĀŗĶH2·“Ó¦Öʱø¼×“¼£ŗCO£Øg£©+2H2£Øg£©?CH3OH£Øg£©£®Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«1molCl2ĶØČėµ½Ė®ÖŠ£¬ŌņN£ØHClO£©+N£ØCl-£©+N£ØClO-£©=2NA | |
| B£® | 100mL 18.4mo1•L-1ĮņĖįÓė×ćĮæCu·“Ó¦£¬Éś³ÉSO2µÄ·Ö×ÓŹżĪŖ0.92NA | |
| C£® | ±ź×¼×“æöĻĀ£¬2.24 LČżĀČ¼×ĶéÖŠŗ¬ÓŠĢ¼ĀČ¹²¼Ū¼üµÄŹżÄæĪŖ0.3NA | |
| D£® | ÓƶčŠŌµē¼«µē½āCuSO4ČÜŅŗŅ»¶ĪŹ±¼äŗó£¬Čō¼ÓČė0.05molµÄCu2£ØOH£©2CO3¹ĢĢåĒ”ŗĆÄÜŹ¹ČÜŅŗ»Öø“µ½ŌĄ“µÄÅØ¶Č£¬ŌņøƵē½ā¹ż³ĢÖŠ×ŖŅʵē×ӵďżÄæĪŖ0.3NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com