
一定条件下,可逆反应X(g)+3Y(g)  2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时,X、Y、Z的浓度分别为0.1 mol/L,0.3 mol/L,0.08 mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时,X、Y、Z的浓度分别为0.1 mol/L,0.3 mol/L,0.08 mol/L,则下列判断不合理的是
A.c1:c2= 1:3 B.X、Y的转化率相等
C.平衡时,Y和Z的生成速率之比为2:3
D.c1的取值范围为0<c1﹤0.14 mol/L
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
下列关系式能说明可逆反应N2(g)+3H2(g)  2NH3(g)已达平衡的是
2NH3(g)已达平衡的是
A、3v正( N2)=v正( H2) B、v正( N2)=v逆( NH3)
C、2v正( H2)=3v逆( NH3) D、v正( N2)=3v逆( H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
A.1∶9 B.1∶1 C.1∶2 D.1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2(g) + Br2(l) = 2 HBr(g) ΔH =-72 kJ/mol,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其它的相关数据如下表:
| H2(g) | Br2(g) | HBr(g) | |
| 1 mol分子中的化学键断裂时需要吸收的能量 / kJ | 436 | a | 369 |
则表中a为
A.404 B.260 C.230 D.200
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在固定容积的密闭容器中发生可逆反应H2(g)+I2(g) 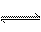 2HI(g)。已知H2和I2的起始浓度均为0.1 mol/L,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均为0.2 mol/L,则平衡时H2的浓度(mol/L)为
2HI(g)。已知H2和I2的起始浓度均为0.1 mol/L,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均为0.2 mol/L,则平衡时H2的浓度(mol/L)为
A.0.16 B.0.08 C.0.04 D.0.02
查看答案和解析>>
科目:高中化学 来源: 题型:
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g)  2N2(g)+3H2O(g) ΔH < 0
2N2(g)+3H2O(g) ΔH < 0
在恒容的密闭容器中,下列有关说法正确的是
A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C.其他条件不变,充入惰性气体,正逆反应速率均不发生变化,平衡不移动
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
用实验确定某酸HA是弱电解质。两同学的方案是:
甲:① 称取一定质量的HA配制0.lmol/L的溶液100mL;
② 用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:① 用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL;
② 分别取这两种溶液各10mL,加水稀释为100mL;
③ 各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)用pH试纸测定HA溶液pH的操作方法为 。
(3)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
(4)乙方案中,说明HA是弱电解质的现象是 (选填编号)。
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验探究:探究碳、硅元素的非金属性的相对强弱,根据要求完成下列各小题:
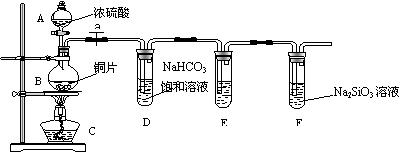 (1)实验装置:
(1)实验装置:
填写所示仪器名称A ; B
(2)实验步骤:
连接仪器、_____________、加药品后,打开a、然后滴入浓硫酸,加热。
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是 ;
装置E中足量酸性KMnO4溶液(具有强氧化性)的作用是 ;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是 ;
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性_ __ (填“能”或“否”),试管D中发生反应的离子方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com