
| ||
| 0.508g |
| 254g/mol |
| 0.004mol |
| 2 |


科目:高中化学 来源: 题型:
| A、① | B、② | C、②③ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
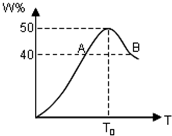 2L容器中,分别将物质的量均为2.00mol的X、Y混合,在不同温度(T)下发生如下反应:2X(g)+Y(g)?2W(g).并在第10s时分别测定其中W的体积分数(W%),并绘成如图所示曲线:
2L容器中,分别将物质的量均为2.00mol的X、Y混合,在不同温度(T)下发生如下反应:2X(g)+Y(g)?2W(g).并在第10s时分别测定其中W的体积分数(W%),并绘成如图所示曲线:. |
| v |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放热反应发生时不必加热,吸热反应在加热后才能发生 |
| B、反应热指的是反应过程中放出的热量 |
| C、反应热的大小与反应的途径有关,无论是一步完成还是分几步完成,其反应热基本相同 |
| D、依据盖斯定律,热化学方程式具有加合性,也可以进行加、减、乘、除四则运算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳和水反应吸收131.3 kJ热量 |
| B、1 mol碳和1 mol水反应生成一氧化碳和氢气,同时放出131.3 kJ热量 |
| C、1 mol碳和1 mol水蒸气反应生成1 mol CO和1 mol H2,同时吸收131.3 kJ热量 |
| D、1个固态碳原子和1分子水蒸气反应吸热131.1 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、汽油、柴油和植物油都是碳氢化合物 |
B、β-月桂烯的结构如图 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
| C、植物油通过加氢可以变为脂肪 |
| D、煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏制取 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、-488.3 kJ/mol |
| B、-244.15 kJ/mol |
| C、+488.3 kJ/mol |
| D、+244.15 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com