
| A.食用碱的主要成分为氢氧化钠 | B.光纤的主要成分为晶体硅 | C.铜绿的主要成分为氢氧化铜 | D.漂白液的有效成分为次氯酸钠 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
分析 A.NaOH为强碱,具有强腐蚀性;
B.光纤的成分为二氧化硅;
C.铜绿的成分为碱式碳酸铜;
D.次氯酸钠具有强氧化性.
解答 解:A.NaOH为强碱,具有强腐蚀性,不能作食用碱,食用碱的主要成分为碳酸氢钠,故A错误;
B.光纤的成分为二氧化硅,二氧化硅具有对光良好的全反射作用,故B错误;
C.铜绿的成分为碱式碳酸铜,而氢氧化铜为蓝色,故C错误;
D.次氯酸钠具有强氧化性,具有漂白性,则漂白液的有效成分为次氯酸钠,故D正确;
故选D.
点评 本题考查物质的性质、应用,为高频考点,把握物质的性质、成分及性质与应用的关系为解答的关键,侧重分析与应用能力的考查,注意判断物质组成和性质,注重元素化合物与生活相结合的训练,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.4 mol | B. | 0.5 mol | C. | 0.6 mol | D. | 0.8 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
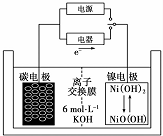
| A. | 充电时阴极发生氧化反应 | |
| B. | 充电时将碳电极与电源的正极相连 | |
| C. | 放电时碳电极反应为H2-2e -=2H+ | |
| D. | 放电时镍电极反应为NiO(OH)+H20+e-=Ni( OH)2+OH - |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 钢铁的电化学腐蚀和化学腐蚀往往同时发生 | |
| B. | 反应C(s)+H2O(g)═CO(g)+H2(g)的△S>0、△H<0 | |
| C. | 常温下,pH为5的氯化铵溶液和pH为9的醋酸钠溶液中水的电离程度相同 | |
| D. | 向BaSO4沉淀中加入饱和Na2CO3溶液后生成BaCO3,则Ksp(BaCO3)<Ksp(BaSO4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=2与pH=1的CH3COOH溶液中c(H+)之比为1:10 | |
| B. | 0.1 mol•L-1的CH3COOH溶液中,由水电离的c(H+)为10-13 mol•L-1 | |
| C. | 常温下,等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,混合后溶液pH<7 | |
| D. | 1.0 mol•L-1Na2CO3溶液:c(OH-)═c(HCO3-)+c(H+)+2c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
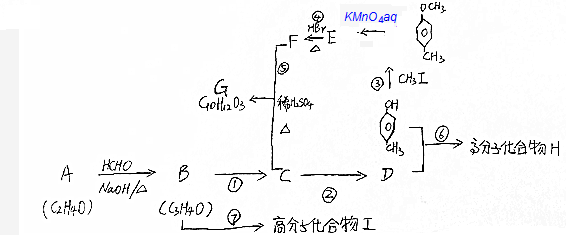

 $\stackrel{KMnO_{4}aq}{→}$
$\stackrel{KMnO_{4}aq}{→}$
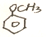 $→_{△}^{HBr}$
$→_{△}^{HBr}$ 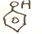
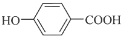 +CH3CH2CH2OH$→_{△}^{浓硫酸}$
+CH3CH2CH2OH$→_{△}^{浓硫酸}$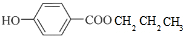 +H2O
+H2O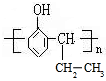
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,H+、Al3+、Cl?能大量共存 | |
| B. | 溶液中c(H2CO3)<c(CO32?) | |
| C. | 该溶液中阳离子总数大于阴离子总数 | |
| D. | 常温下,加水稀释,$\frac{c({H}^{+}).c(C{O}_{3}^{2-})}{c(HC{O}_{3}^{-})}$变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
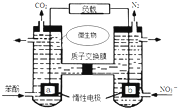
| A. | a电极发生还原反应,做原电池的正极 | |
| B. | b电极反应式为:2NO3-+10e-+12H+═N2↑+6H2O | |
| C. | H+由右室通过质子交换膜进入左室 | |
| D. | 标准状况下,电路中产生6moLCO2同时产生22.4L的N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)
.W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com