
溴及其化合物广泛用在有机合成、化学分析等领域。
(1)海水提溴过程中溴元素的变化如下 :
:
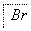
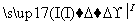
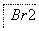
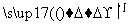
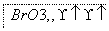
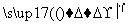
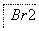
①过程Ⅰ,海水显碱性,调其pH<3.5后,再通入氯气。
ⅰ.通入氯气后,反应的离子方程式是_______________________。
ⅱ.调海水pH可提高Cl2的利用率,用平衡原理解释其原因是______。
②过程Ⅱ,用热空气将溴赶出,再用浓碳酸钠溶液吸收。完成并配平下列方程式。
 Br2+
Br2+ Na2CO3===
Na2CO3=== NaBrO3+
NaBrO3+ CO2+
CO2+ ________
________
③过程Ⅲ,用硫酸酸化可得Br2和Na2SO4的混合溶液。
相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是__________是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入2.6 mol NaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
| 粒子 | I2 | Br2 | IO |
| 物质的量/mol | 0.5 | 1.3 |
则原溶液中NaI的物质的量为________mol。
解析 (1)①ⅱ.氯气与水的反应是可逆反应:Cl2+H2OH++Cl-+HClO,海水呈碱性可使该平衡正向移动,则与Br-发生反应的氯气减少,造成氯气的利用率降低。所以调节海水的pH<3.5,使之呈酸性,从而抑制氯气发生副反应。②完成方程式的依据:得失电子守恒和
元素守恒。③BrO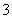 具有强氧化性,能将Cl-氧化,造成溴元素的损失。(2)反应的离子方程式为I-+BrO
具有强氧化性,能将Cl-氧化,造成溴元素的损失。(2)反应的离子方程式为I-+BrO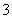 ―→I2+Br2+IO
―→I2+Br2+IO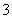 (未参与电子转移的物质未列出),设生成物中IO
(未参与电子转移的物质未列出),设生成物中IO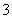 的物质的量为x mol,由得失电子守恒得:0.5×2×[0-(-1)]+x×[5-(-1)]=2.6×(5-0),解得x=2。再由碘元素守恒可知原溶液中NaI的物质的量为3 mol。
的物质的量为x mol,由得失电子守恒得:0.5×2×[0-(-1)]+x×[5-(-1)]=2.6×(5-0),解得x=2。再由碘元素守恒可知原溶液中NaI的物质的量为3 mol。
答案 (1)①ⅰ.Cl2+2Br-===Br2+2Cl-
ⅱ.通入Cl2后发生反应Cl2+H2OH++Cl-+HClO,增大c(H+),平衡逆向移动,抑制Cl2与水反应
②3 3 1 3 5 NaBr ③盐酸有还原性,与溴酸根离子反应 (2)3


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
控制适合的条件,将反应2Fe3++2I-=2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是( )
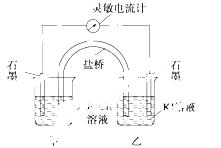 A.反应开始时,乙中石墨电极上发生氧化反应
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中的石墨电极为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
与MnO2Zn电池类似,K2FeO4Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应为____________,该电池总反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
新型高效 的甲烷燃料电池采用铂为
的甲烷燃料电池采用铂为 电极材料,两电极上分别通入CH4和O2 ,
电极材料,两电极上分别通入CH4和O2 ,
电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如
图所示。
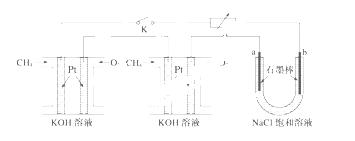
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为______ __________、____________________。
__________、____________________。
(2)闭合K开关后,a、b电极上均有气体产生,其中b电极上得到的是__________,电解氯化钠溶液的总反应方程式为__________________________________________________________;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为__________(法拉第常数F=9.65×104 C · mol-1列式计算),最多能产生的氯气体积为________L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项反应对应的图象错误的是( )
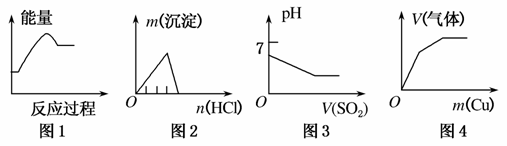
A.图1:将氮气和氧气混合后在放电条件下反应
B.图2:将稀盐酸逐滴加入一定量偏铝酸钠溶液中
C.图3:将二氧化硫逐渐通入一定量氯水中
D.图4:将铜粉逐渐加入一定量浓硝酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
对Na、Mg、Al的有关性质的叙述正确的是 ( )
A.碱性:NaOH<Mg(OH)2<Al(OH)3
B.第一电离能:Na<Mg<Al
C.电负性:Na>Mg>Al
D.还原性: Na>Mg>Al
Na>Mg>Al
查看答案和解析>>
科目:高中化学 来源: 题型:
“嫦娥一号”卫星在北京航天飞机控制中心科技人员的精确控制下,准确落于月球东经52.36°、南纬1.50°
的预定撞击点。“嫦娥一号”担负的四大科学目标之一是探测下列14种元素的含量和分布情况:K、Th(钍)、
U(铀)、O 、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn、Cr(铬)、Gd(钆),其中属于主族元素的有( )
、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn、Cr(铬)、Gd(钆),其中属于主族元素的有( )
A.4种 B.5 种 C.6种 D.7种
种 C.6种 D.7种
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可
与其最高价含氧酸反应生成离子化合物,由此可知
| W | X | |
| Y | Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W四种短周期主族元素在周表中的相对位置如图所示,下列说法正确的是 ( )
| X | Y |
| Z | W |
A.W的原子序数可能是Y的原子序数的2倍
B.Z元素的原子半径可能比Y元素的小
C.W的气态氢化物的稳定性一定 比Y的强
比Y的强
D.Z的化学活泼性一定比X强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com