
| m |
| M |
| ma+nb |
| m+n-p |
| 1000ρω |
| M |
| 38g |
| 0.4mol |
| ma+nb |
| m+n-p |
| 1000ρω |
| M |
| 1000ρω |
| c |
1000×q×
| ||
| c |
| 1000q(am+nb) |
| c(m+n-p) |
| 1000q(am+nb) |
| c(m+n-p) |
| 1000q(am+nb) |
| c(m+n-p) |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、丁达尔现象不是胶体特有的,溶液也具备 |
| B、欲配制1.00 L 1.00 mol?L-1的NaCl溶液,可将58.5g NaCl溶于1.00 L水中 |
| C、质子数为53,中子数为78的碘原子可表示为:131 53I |
| D、煤的干馏和石油的分馏均属化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?L-1的NH4Cl溶液C(Cl-)>C(NH4+)>C(OH-)>C(H+) |
| B、0.1mol?L-1的(NH4)2SO4溶液中:C(NH4+)=2 C(SO42-) |
| C、0.2mol?L-1的Na2CO3溶液中:C(OH-)=C(HCO3-)+C(H+)+C(H2CO3) |
| D、C(NH4+)相等的NH4HSO4溶液,NH4HCO3溶液和NH4Cl溶液中,C(NH4H SO4)<C( NH4Cl)<C(NH4HCO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、食盐中阴离子的结构示意图为: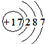 |
| B、蔗糖和醋酸都是弱电解质 |
C、“84消毒液”中有效成分NaClO的电子式为: |
| D、明矾溶液水解可制得Al(OH)3胶体,用于杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | C≡O (CO) | C=O | H-O | H-H |
| 键能(kJ?mol-1) | 1070 | 801 | 463 | 436 |
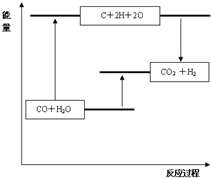 B.
B.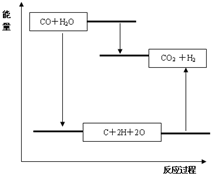
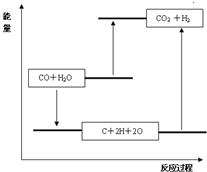 D.
D.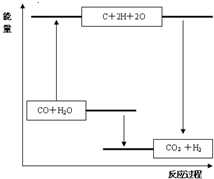
| 1 |
| 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com